
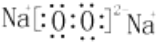
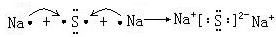
 、其最高价氧化物对应的水化物的化学式H3PO4.
、其最高价氧化物对应的水化物的化学式H3PO4. 分析 (1)过氧化钠中两个氧原子通过共用电子对结合,两个钠离子与过氧根离子通过离子键结合;
(2)硫化钠为离子化合物,根据离子化合物的电子式结合电子转移然后写出Na2S的形成过程;
(3)元素符号左下角数字表示质子数、左上角数字表示质量数;
(4)空气中含量最多的气体是氮气,氮气分子中两个氮原子共用3对电子;
(5)氯化铵为离子化合物,存在铵根离子与氯离子之间的离子键、氮原子与氢原子之间的共价键;次氯酸钠为离子化合物,存在钠离子与次氯酸根离子离子键,氯原子与氧原子之间的共价键;
(6)原子序数为15的原子为磷原子;最高价氧化物对应的水化物的化学式H3PO4;
解答 解:(1)过氧化钠为离子化合物,2个钠离子与过氧根离子通过离子键结合,两个氧原子通过共用电子对结合,电子式为: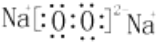 ;
;
故答案为: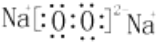 ;
;
(2)硫化钠为离子化合物,一个钠原子失去一个电子,一个硫原子得到两个电子,则用电子式表示Na2S的形成过程为: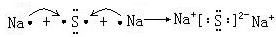 .
.
故答案为: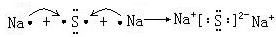 ;
;
(3)元素符号左下角数字表示质子数、左上角数字表示质量数,硫离子:3416S2-,
故答案为:3416S2-;
(4)空气中含量最多的气体是氮气,氮气分子中两个氮原子共用3对电子,结构式:N≡N,
故答案为:N≡N;
(5)氯化铵为离子化合物,存在铵根离子与氯离子之间的离子键、氮原子与氢原子之间的共价键;次氯酸钠为离子化合物,存在钠离子与次氯酸根离子离子键,氯原子与氧原子之间的共价键;
所以二者都含有的是:离子键、共价键;
故答案为:离子键、共价键;
(6)原子序数为15的原子为磷原子,原子结构示意图 ;最高价氧化物对应的水化物的化学式H3PO4,
;最高价氧化物对应的水化物的化学式H3PO4,
故答案为: ;H3PO4;
;H3PO4;
点评 本题考查了,电子式、离子符号、原子结构示意图的书写,结构式,明确物质的结构及电子式书写的方法是解题关键,侧重考查学生对常用化学用语书写的规范性,题目难度不大.


 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  :3-甲基-2-戊烯 :3-甲基-2-戊烯 | B. | 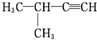 :2-甲基-3-丁炔 :2-甲基-3-丁炔 | ||
| C. | 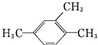 :1,3,4-三甲苯 :1,3,4-三甲苯 | D. | 2,3-二甲基-2-乙基己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Br的电子式: | |
| B. | S2-的结构示意图: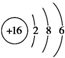 | |
| C. | 原子核内有18个中子的氯分子${\;}_{17}^{35}$Cl2 | |
| D. | CS2分子的结构式:S-C-S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①式表示常温常压时,2 mol H2和1 mol O2完全燃烧生成2 mol H2O(l)放热571.6 kJ | |
| B. | 2H2(g)+O2(g)=2H2O(g)中△H大于-571.6 kJ•mol-1 | |
| C. | 将含1 mol NaOH的水溶液与50 g 98%的硫酸溶液混合后放出的热量大于57.3 kJ | |
| D. | 将含1 mol NaOH的稀溶液与含1 mol CH3COOH的稀溶液混合后放出的热量为57.3 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | HF、HCl、HBr、HI的沸点依次升高 | B. | HF、HCl、HBr、HI还原性依次增强 | ||
| C. | HF、HCl、HBr、HI稳定性依次增强 | D. | HF、HCl、HBr、HI酸性依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水玻璃中加入稀盐酸:Na2SiO3+2H+=H2SiO3↓+2Na+ | |
| B. | 铝与稀硝酸反应:2Al+6H+═2Al3++3H2↑ | |
| C. | 氯化铝溶液和过量氨水反应:Al3++3NH3•H2O═3NH4++Al (OH)3↓ | |
| D. | 向硅酸钠溶液中通入过量二氧化碳:SiO32-+CO2+H2O═H2SiO3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com