
| ѡ�� | ʵ����� | �۲���¼ | ���ۻ���� |
| A | ��Ũ����ֶ�μ���Cu��ϡ����Ļ��Һ�� | ��������ɫ���� | Ũ����Ļ�ԭ������NO2 |
| B | ��ij�����Һ��pH | pH��7 | NH4+ˮ������NH3•H2O��ʹ��Һ�Լ��� |
| C | ��ʪ��ĵ��۵⻯����ֽ����ij���� | ��ֽ���� | ������һ����Cl2 |
| D | ��ʢ����ˮ�ķ�Һ©�����á����á���������ת1800���ٴε��� | ©���ںͻ�����©ˮ | ��Һ©����©Һ |
| A�� | A | B�� | B | C�� | C | D�� | D |
���� A��һ����������������Ӧ���ɶ���������
B��NH4+ˮ�������ԣ�
C����ʹʪ��ĵ��۵⻯����ֽ������˵����Ӧ���е��ʵ����ɣ���˸�������������ԣ�
D�����Ͽ�ƿ����ת180�ȣ����ŵ��ţ����¶�������ת180�ȣ����ŵ��ţ�������©ˮ�����Һ©����©ˮ��
��� �⣺A��ϡ����Ļ�ԭ������һ��������һ����������������Ӧ���ɶ�����������A����
B��NH4+ˮ�������ԣ�pH��7����B����
C���������Ե����ʲ�һ������������C����
D����Һ©����װ����������ˮ�����ţ����ţ����Ͽ�ƿ����ת180�ȣ����ŵ��ţ����¶�������ת180�ȣ����ŵ��ţ�������©ˮ�����Һ©����©ˮ����D��ȷ��
��ѡD��
���� ���⿼�黯ѧʵ�鷽�������ۣ�Ϊ��Ƶ���㣬�漰ʵ��������������ʵ����ʵȣ�����ʵ������Ĺ淶�ԡ�ʵ��ϸ�ں�ʵ��ԭ��Ϊ���Ĺؼ���ע�ⷽ���ĺ����ԡ������ԡ������Է�������Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��5 mL 0.02 mol/L��H2SO4��Һ��5 mL 0.02 mol/L NaOH��Һ��ֻ�ϣ�����Ϻ���Һ�����Ϊ10 mL������Һ��pH=2 | |
| B�� | ij���ʵ���Һ����ˮ�����c��H+��=1��10-a mol/L����a��7����pHһ��Ϊ14-a | |
| C�� | pH��ȵĢ�CH3COONa ��C6H5ONa ��NaHCO3��Һ��c��Na+����С��ϵ���٣��ۣ��� | |
| D�� | CH3COONa��Һ�м�������KNO3�����ļ�����Һһ���У�c��Na+��+c��H+��=c��CH3COO-��+c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ˮԭ��Ϊ��Al3++3H2O=Al��OH��3��+3H+ | |
| B�� | ����Һ��AlO2-��F-��K+��Na+�ܴ������� | |
| C�� | �������NH3•H2O��Ӧ�����ӷ���ʽΪ��Al3++4NH3•H2O=AlO2-+4NH4++2H2O | |
| D�� | �������Ba��OH��2��Һ��Ӧ�����ӷ���ʽΪ��Al3++2SO42-+4OH-+2Ba2+=AlO2-ʮ2BaSO4��+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
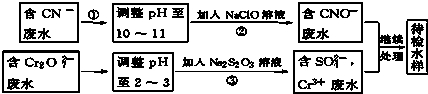
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ԫ��A���γɵ��⻯�ﳣ����һ��Ϊ��̬ | |
| B�� | �ǽ����ԣ�A��E | |
| C�� | Ԫ��C��D��E����Ȼ���о�����������̬���� | |
| D�� | Ԫ��B���������Ӧ��ˮ����һ��Ϊǿ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
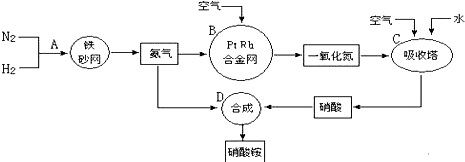
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 6�� | B�� | 7�� | C�� | 8�� | D�� | 9�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
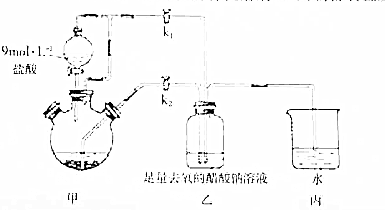 �ټ��װ�������Ժ���������ƿ�����μ������п��������CrCl3��Һ��
�ټ��װ�������Ժ���������ƿ�����μ������п��������CrCl3��Һ�� �鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com