
 按要求对如图中两极进行必要的连接并填空:
按要求对如图中两极进行必要的连接并填空:

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、石油是混合物,汽油是纯净物 |
| B、石油的分馏是物理变化,煤的干馏也是物理变化 |
| C、分馏石油气和裂化石油气的成分一样 |
| D、石油的裂化和裂解是化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某同学查资料得知α-AgI是一种固体导体,导电率很高.他为了研究α-AgI究竟是Ag+离子导电还是I-离子导电,设计一个如图所示(用铅蓄电池做电源)的电化学实验.
某同学查资料得知α-AgI是一种固体导体,导电率很高.他为了研究α-AgI究竟是Ag+离子导电还是I-离子导电,设计一个如图所示(用铅蓄电池做电源)的电化学实验.| 放电 |
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
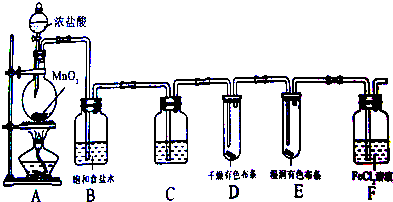
查看答案和解析>>
科目:高中化学 来源: 题型:
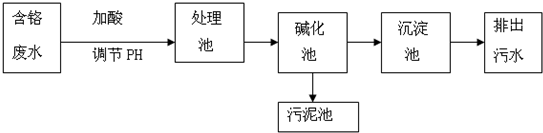
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化硼液态时能导电而固态时不导电 |
| B、氯化硼加到水中使溶液的pH升高 |
| C、氯化硼分子呈平面正三角形,属非极性分子 |
| D、氯化硼B-Cl之间是sp3形成的σ键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、甲烷与氯气制备一氯甲烷 |
| B、乙烯聚合为聚乙烯高分子材料 |
| C、以铜和浓硝酸为原料生产硝酸铜 |
| D、用苯和浓硝酸反应制取硝基苯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com