
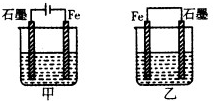
 如图所示装置,均盛有等体积等浓度的稀硫酸,工作一段时间后当甲乙装置中通过电子的物质的量相同时,下列说法正确的是( )
如图所示装置,均盛有等体积等浓度的稀硫酸,工作一段时间后当甲乙装置中通过电子的物质的量相同时,下列说法正确的是( )| A. | A、甲乙两装置中的石墨电极分别是阴极、负极 | |
| B. | 铁棒的腐蚀程度:甲>乙 | |
| C. | 石墨电极上发生反应的电极反应式相同 | |
| D. | 溶液的pH:甲减小,乙增大 |
分析 A、甲中石墨电极与电源的正极相连,乙中的石墨是正极;
B、作原电池负极的金属加速被腐蚀,作电解池阴极的金属被保护;
C、甲中石墨电极上氢氧根离子放电生成氧气,乙中石墨电极上氢离子放电生成氢气;
D、甲中电池反应式为2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑、乙中电池反应式为Fe+2H+=H2↑+Fe2+.
解答 解:A、甲中石墨电极与电源的正极相连,所以是阳极,而乙中的石墨是正极,故A错误;
B、甲中Fe作阴极,被保护,乙中铁作负极被腐蚀,所以铁棒的腐蚀程度:甲<乙,故B错误;
C、甲中石墨电极上氢氧根离子放电生成氧气,乙中石墨电极上氢离子放电生成氢气,所以二者电极反应式不同,故C错误;
D、甲中电池反应式为2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑、乙中电池反应式为Fe+2H+=H2↑+Fe2+,甲中硫酸浓度增大、乙中硫酸浓度减小,所以溶液的pH:甲减小,乙增大,故D正确;
故选D.
点评 本题考查了原电池和电解池原理,明确各个电极上发生的反应即可解答,会正确书写电极反应式,题目难度不大.


科目:高中化学 来源: 题型:选择题
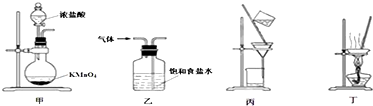
| A. | 用装置甲制取氯气 | |
| B. | 用装置乙除去氯气中的少量氯化氢 | |
| C. | 用装置丙分离二氧化锰和氯化锰溶液 | |
| D. | 用装置丁蒸发浓缩氯化锰溶液,冷却可得MnCl2•4H2O晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑥ | B. | ④⑥ | C. | ②③④ | D. | ②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 室温下,氨水与氯化铵的pH=7的混合溶液中:c(Cl-)=c(NH4+) | |
| B. | 向NaHCO3溶液中加入少量NaOH固体,可抑制HCO3-的水解,使c(HCO3-)增大 | |
| C. | 0.1 mol•L-1的(NH4)2SO4溶液中:c(NH4+)>c(SO42-)>c(H+)>c(OH-) | |
| D. | 常温下,等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和时,a+b=14 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上常通过电解熔融的MgO冶炼金属镁 | |
| B. | 应用盖斯定律,可计算某些难以直接测量的反应焓变 | |
| C. | 用惰性电极电解Na2SO4溶液,阴、阳两极产物的物质的量之比为1:2 | |
| D. | 在铁上镀铜,应选用铜作阴极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、OH-、H3O+ | B. | Na+、Mg2+、S2- | C. | F-、NH2-、Cl- | D. | Li+、Na+、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M、N全部变成了Q | |
| B. | M、N、Q三种物质的浓度一定相等 | |
| C. | 反应已经停止 | |
| D. | 反应混合物各成分的百分组成不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、Na+、NO3-、Cl- | B. | K+、Na+、Cl-、CO32- | ||
| C. | NH4+、Na+、Cl-、SO42- | D. | NH4+、K+、SiO32-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C和O2 | B. | Na2CO3和盐酸 | C. | Na和O2 | D. | NaHCO3和NaOH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com