
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案科目:高中化学 来源: 题型:
下列事实不能用勒夏特列原理解释的是:
A.氯水中有平衡:Cl2+H2O HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅。
HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅。
B.对CO(g)+NO2(g)  CO2(g)+NO(g),平衡体系增大压强可使颜色变深。
CO2(g)+NO(g),平衡体系增大压强可使颜色变深。
C.升高温度能够促进水的电离
D.SO2催化氧化成SO3的反应,往往加入过量的空气
查看答案和解析>>
科目:高中化学 来源: 题型:
 l,2二溴乙烷可作汽油抗爆剂的添加剂,常温 下它是无色液体,密度2.189.cm
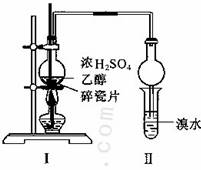
l,2二溴乙烷可作汽油抗爆剂的添加剂,常温 下它是无色液体,密度2.189.cm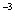 ,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在 实验室中可用下列反应制备1,2二溴乙烷。
,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。在 实验室中可用下列反应制备1,2二溴乙烷。

某化学兴趣小组用如图所示的装置(部分固定和夹持装置省略)进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性。当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓硫酸与乙醇的混合液体变为棕黑色。
回答下列问题:
(1)已知该实验的副反应之一是乙醇会被浓硫酸氧化成CO2。写出该反应的化学方程式:
_________________________________________________________________。
(2)甲同学认为:溴水褪色的现象不能证明反应中有乙烯生成且乙烯具有不饱和性,其理
由是________(填正确答案的标号,下同)。
A.乙烯与溴水易发生取代反应 B.使溴水褪色的物质,未必是乙烯
C.使溴水褪色的反应,未必是加成反应
D.浓硫酸氧化乙醇生成的乙醛,也会使溴水褪色
(3)乙同学经过仔细观察后认为试管中另一现象可证明反应中有乙烯生成,该现象是
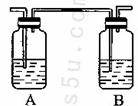 (4)丙同学对上述实验进行了改进,在I和II之间增加如图所示的装置,则A中的试剂为________,其作用是________B中的试剂为________,其作用是________。
(4)丙同学对上述实验进行了改进,在I和II之间增加如图所示的装置,则A中的试剂为________,其作用是________B中的试剂为________,其作用是________。
(5)丁同学通过洗涤、蒸馏等操作对l,2一二溴乙烷粗品进行了精制。该洗涤操作用到的主要玻璃仪器是_________,该仪器在使用前须清洗干净并_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能说明非金属性Cl>I的是( )
A.Cl2+2I-==2Cl-+I2 B.稳定性:HCl>HI
C.酸性 HClO4>HIO4 D.酸性 HClO3>HIO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于同系物的说法中,不正确的是 ( )
A.同系物具有相同的最简式
B.同系物能符合同一通式
C.同系物中,相邻的同系物彼此在组成上相差一个CH2原子团
D.同系物的化学性质基本相似,物理性质随碳原子数增加而呈规律性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A. 催化剂可以使不起反应的物质发生反应
B. 决定化学反应速率的主要因素是参加反应的物质的性质
C. 可以找到一种催化剂使水变成油
D. 催化剂是决定化学反应速率的主要因素
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是 ( )
A.铁是人类在生产、生活中最早使用的金属材料
B.金、银、铜是应用最广泛的金属材料
C.钛被誉为“21世纪的金属”,应用前景很广阔
D.铜是导电性、导热性最好的有色金属
查看答案和解析>>
科目:高中化学 来源: 题型:
最近雾霾天气又开始肆虐我国大部分地区。其中SO2是造成空气污染的主要原因,利用钠碱循环法可除去SO2。
(1)钠碱循环法中,吸收液为Na2SO3溶液,该吸收反应的离子方程式是________________。
(2)已知H2SO3的电离常数为K1=1.54×10-2,K2=1.02×10-7,H2CO3的电离常数为K1=4.30×10-7,K2=5.60×10-11,则下列微粒可以共存的是 ________________。
A.CO HSO
HSO B.HCO
B.HCO HSO
HSO
C.SO HCO
HCO D.H2SO3 HCO
D.H2SO3 HCO
(3)吸收液吸收SO2的过程中,pH随n(SO ):n(HSO
):n(HSO )变化关系如下表:
)变化关系如下表:
| n(SO | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
①上表判断NaHSO3溶液显________________性,从原理的角度解释原因________________。
②在NaHSO3溶液中微粒浓度关系不正确的是________(选填字母)。
A.c(Na+)=2c(SO )+c(HSO
)+c(HSO )
)
B.c(Na+)>c(HSO )>c(H+)>c(SO
)>c(H+)>c(SO )>c(OH-)
)>c(OH-)
C.c(H2SO3)+c(H+)=c(SO )+c(OH-)
)+c(OH-)
D.c(Na+)+c(H+)=2c(SO )+c(HSO
)+c(HSO )+c(OH-)
)+c(OH-)
(4)当吸收液的pH降至约为6时,需送至电解槽再生。再生示意图如下:
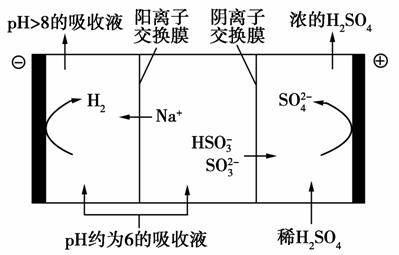
①吸收液再生过程中的总反应方程式是________________。
②当电极上有1 mol电子转移时阴极产物为________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com