
 O2(g)=H2O(l)△H=-285.84kJ?mol-1
O2(g)=H2O(l)△H=-285.84kJ?mol-1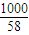 mol,完全燃烧并生成二氧化碳和液态水时,放出热量为5×104kJ,所以1mol丁烷完全燃烧生成稳定氧化物时放出的热量为5×104kJ×
mol,完全燃烧并生成二氧化碳和液态水时,放出热量为5×104kJ,所以1mol丁烷完全燃烧生成稳定氧化物时放出的热量为5×104kJ×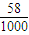 =2900kJ,燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出的热量,表示丁烷燃烧热的热化学方程式:C4H10(g)+
=2900kJ,燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出的热量,表示丁烷燃烧热的热化学方程式:C4H10(g)+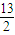 O2(g)═4CO2(g)+5H2O;△H=-2900kJ/mol;
O2(g)═4CO2(g)+5H2O;△H=-2900kJ/mol;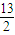 O2(g)═4CO2(g)+5H2O;△H=-2900kJ/mol;
O2(g)═4CO2(g)+5H2O;△H=-2900kJ/mol; ②+③得到:Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=-319.68KJ/mol,
②+③得到:Cu(s)+H2O2(l)+2H+(aq)=Cu2+(aq)+2H2O(l)△H=-319.68KJ/mol,

科目:高中化学 来源: 题型:
| 1 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 13 |
| 2 |
| 13 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2012-2013学年浙江省台州中学高二下学期期中考试化学试卷(带解析) 题型:填空题
(1)家用液化气的主要成分之一是丁烷(C4H10),当2 mol丁烷完全燃烧生成二氧化碳和液态水时,放出热量为5800kJ,试写出表示丁烷燃烧热的热化学方程式: ;
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)="=" 2Fe(s)+3CO2(g) ΔH =" -24.8" kJ·mol-1
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) ΔH =" -47.4" kJ·mol-1
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H =" +640.5" kJ·mol-1
写出CO(g)还原FeO(s)得到Fe (s)和CO2(g)的热化学反应方程式 。
查看答案和解析>>
科目:高中化学 来源:2013届浙江省高二下学期期中考试化学试卷(解析版) 题型:填空题
(9分)
(1)家用液化气的主要成分之一是丁烷(C4H10),当1 kg丁烷完全燃烧生成二氧化碳和液态水时,放出热量为5×104kJ,试写出表示丁烷燃烧热的热化学方程式:
(2)已知:C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ·mol-1
现有0.2 mol的炭粉和氢气组成的悬浮气,且混合物在氧气中完全燃烧,共放出63.53 kJ热量,则混合物中C与H2的物质的量之比为
(3)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)== 2Fe(s)+3CO2(g) △H=—24.8 kJ·mol-1
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H=—47.4 kJ·mol-1
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= +640.5 kJ·mol-1
写出CO(g)还原FeO(s)得到Fe (s)体和CO2(g)的热化学反应方程式:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com