
| A. | PH3 分子是非极性分子 | |
| B. | PH3分子中有一对电子孤对 | |
| C. | PH3 分子VSEPR模型的名称是四面体 | |
| D. | PH3 分子稳定性低于 NH3 分子 |
分析 A.分子结构是三角锥型,正负电荷重心不重合,为极性分子;
B.PH3 分子结构和 NH3 相似;
C.价层电子对互斥模型(简称VSEPR模型),根据价电子对互斥理论,价层电子对个数=σ键个数+孤电子对个数.σ键个数=配原子个数,孤电子对个数=$\frac{1}{2}$×(a-xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数;
D.共价键键长越短,键能越大,分子越稳定.
解答 解:A.PH3分子结构是三角锥型,正负电荷重心不重合,为极性分子,故A错误;
B.PH3 分子结构和 NH3 相似,中心原子都含有一个孤电子对,故B正确;
C.PH3分子中价层电子对个数=σ键个数+孤电子对个数=3+$\frac{1}{2}$(5-3×1)=4,VSEPR模型为四面体结构;含有一个孤电子对,所以其空间构型为三角锥形,故C正确;
D.共价键键长越短,键能越大,分子越稳定,P-H键键能比N-H键键能低,是因为P的原子半径比N大,P-H键长比N-H长,则N-H键键长更短、键能更高,所以PH3分子稳定性低于NH3分子,故D正确;
故选A.
点评 本题考查了化学键、分子构型等,会利用知识迁移法进行分析解答,注意价层电子对互斥模型(简称VSEPR模型)理解,和氨气类推性质比较,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
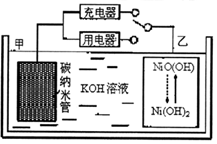 2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户.用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示.下列说法正确的是( )
2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户.用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示.下列说法正确的是( )| A. | 电池总反应为H2+2NiOOH$?_{放电}^{充电}$2Ni(OH)2 | |
| B. | 放电时,甲电极为负极,OH-移向乙电极 | |
| C. | 放电时,乙电极反应为:NiO(OH)+H2O+e-═Ni(OH)2+OH- | |
| D. | 充电时,电池的碳电极与直流电源的正极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 提出问题 | 收集资料 | 提出假设 | 验证假设 | 得出结论 |
| 氯水中何种物质能使湿润的红色布条褪色? | ①氯气有强氧化性 ②氯气与冷水反应生成盐酸和次氯酸 ③次氯酸有强氧化性 | ①氯气使布条褪色 ②盐酸使布条褪色 ③次氯酸使布条褪色 ④H2O使布条褪色 | 实验①:把红色干布条放入充满氯气的集气瓶中,布条不褪色; 实验②:把红色布条伸入稀盐酸中,红色布条不褪色 实验③:把红色布条伸入氯水中,红色布条褪色 实验④:把红色布条放在水里,布条不褪色. | 结论: 次氯酸使布条褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石英是制造光导纤维的原料,也是常用的半导体材料 | |
| B. | 氧化铝是冶炼金属铝的原料,也是较好的耐火材料 | |
| C. | 天然氨基酸能溶于强碱或强酸溶液,是两性化合物 | |
| D. | 船舶外壳装上锌块,是牺牲阳极的阴极保护法进行防腐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷在空气中完全燃烧 | |
| B. | 在镍做催化剂的条件下,苯与氢气反应 | |
| C. | 乙烯通入溴水中 | |
| D. | 乙醇与乙酸制备乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 按系统命名法,有机物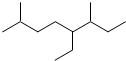 可命名为3,7-二甲基-4-乙基辛烷 可命名为3,7-二甲基-4-乙基辛烷 | |
| B. | 环己醇分子中所有的原子可能共平面 | |
| C. | 麻黄碱(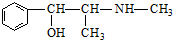 )的催化氧化产物能发生银镜反应 )的催化氧化产物能发生银镜反应 | |
| D. | 某分子式为C10H20O2的酯可发生如图所示的转化过程,则符合条件的酯的结构有4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | F、Cl、Br、I原子半径依次增大 | |
| B. | F、Cl、Br、I的电子层数逐渐增多 | |
| C. | F2、Cl2、Br2、I2的氧化性逐渐减弱 | |
| D. | F-、Cl-、Br -、I-离子的还原性依次减弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com