
根据下表回答问题:
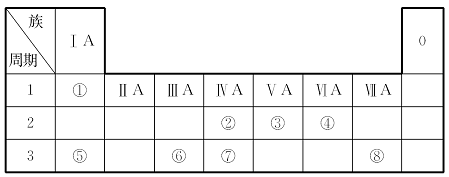
(1)元素⑦在周期表中的位置是___________________。
(2)元素①和⑤的原子序数相差 。
(3)写出元素⑤形成的常见化合物与元素⑧形成的单质反应的化学方程式____
__________________________。
(4)写出元素③形成的不同化合价的化合物的化学式(写出四个)____________
___________________________________________________________________,
其中能与元素⑥形成的单质反应的化学方程式为_________________________
__________________________________________________________________。
科目:高中化学 来源: 题型:
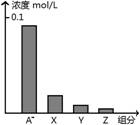
常温下,0.2 mol/L的一元酸.HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )
A.HA为强酸
B.该混合液pH=7
C.图中X表示HA,Y表示OH-,Z表示H+
D.该混合溶液中:c(A-)+c(Y) =c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
①在热化学方程式中无论是反应物还是生成物都必须标明状态
②所有的化学反应都伴随着能量变化
③放热反应发生时不必加热
④吸热反应在加热后才能发生
⑤化学反应的热效应数值只与参加反应的物质的多少有关
⑥一般来说,吸热反应在一定条件下也能发生
A.②③⑥ B.③④⑤
C.④⑤ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
下图为常温下用0.10mol·L-1NaOH溶液滴定20.00 mL 0.10 mol·L-1盐酸和20.00 mL 0.10 mol·L-1醋酸的曲线。若以HA表示酸,下列判断和说法正确的是
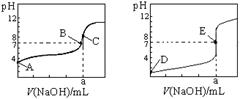
A.左图是滴定盐酸的曲线
B.E点时溶液中离子浓度为c(Na+) = c(A—)
C.B点时,反应消耗溶液体积:V(NaOH)>V(HA)
D.当0mL<V(NaOH)<20. 00mL时,溶液中一定是c(A-)>c(Na+)>c(H+) >c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是 ( )
A.元素的原子序数越大,其族序数也越大
B.同周期的第ⅡA族与第ⅢA族的原子序数一定相差1
C.在元素周期表中,第14列元素所形成的化合物种类最多
D.元素的最外层电子数为奇数,其族序数不一定为奇数
查看答案和解析>>
科目:高中化学 来源: 题型:
已知H—H键键能(断裂时吸收或生成时释放的能量)为436 kJ·mol-1,N—H键键能为391 kJ·mol-1,根据热化学方程式:N2(g)+3H2(g)===2NH3(g) ΔH=-92.4 kJ·mol-1。则N≡N键的键能是( )
A.431 kJ·mol-1 B.945.6 kJ·mol-1
C.649 kJ·mol-1 D.896 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
某学习小组设计以下实验,探究化学反应
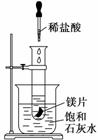
中的热效应,把试管放入盛有25℃的饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管往其中滴加5 mL盐酸。试回答下列问题:
实验中观察到的现象是________________________________________________
________________________________________________________________________
________________________________________________________________________。
(2)产生上述现象的原因是_________________________________________________。
(3)写出有关反应的离子方程式:___________________________________________。
(4)由实验推知,MgCl2和H2的总能量______(填“大于”、“小于”或“等于”)镁片和盐酸的总能量。
(5)如果将本题中“25℃的饱和石灰水”换成“20℃碳酸饮料”进行实验探究,实验中观察到的另一现象是______________________________________________________
________________________________________________________________________
______________________,其原因是____________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对化学反应热问题的说法正确的是( )
A.放热反应发生时不必加热
B.化学反应一定有能量变化
C.一般地说,吸热反应加热后才能发生
D.化学反应的热效应数值与参加反应的物质的多少无关
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E五种短周期主族元素,原子序数由A到E逐渐增大。
①A元素最外层电子数是次外层电子数的2倍。
②B的阴离子和C的阳离子与氖原子的电子层结构相同。
③在通常状况下,B的单质是气体,0.1 mol B的气体与足量的氢气完全反应共有0.4 mol电子转移。
④C的单质在点燃时与B的单质充分反应,生成淡黄色的固体,此淡黄色固体能与AB2反应生成B的单质。
⑤D的气态氢化物与其最高价含氧酸间能发生氧化还原反应。
请写出:
(1)A元素的最高价氧化物的电子式 。
(2)B元素在周期表中的位置 。
(3)B单质与C单质在点燃时反应的生成物中所含化学键类型有 。
(4)D元素的低价氧化物与E的单质的水溶液反应的化学方程式为
。
(5)C与D能形成原子个数比为2∶1的化合物,用电子式表示该化合物的形成过程 。
(6)元素D与元素E相比,非金属性较强的是 (用元素符号表示),下列表述中能证明这一事实的是 (填选项序号)。
a.常温下D的单质和E的单质状态不同
b.E的氢化物比D的氢化物稳定
c.一定条件下D和E的单质都能与钠反应
d.D的最高价含氧酸酸性弱于E的最高价含氧酸
e.D的单质能与E的氢化物反应生成E单质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com