
【题目】下列说法正确的是
A. 已知0.1 mol·L-1的醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,加少量烧碱溶液可使溶液中c(H+)/c(CH3COOH)值增大。
CH3COO-+H+,加少量烧碱溶液可使溶液中c(H+)/c(CH3COOH)值增大。
B. 25 ℃时,向水中加入少量固体CH3COONa,水的电离平衡:H2O![]() H++OH-逆向移动,c(H+)降低
H++OH-逆向移动,c(H+)降低
C. 取c(H+)=0.01 mol·L-1的盐酸和醋酸各100 mL,分别稀释2倍后,再分别加入0.03 g锌粉,在相同条件下充分反应,醋酸与锌反应的速率大
D. 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液中:c(Na+)<c(NO3- )
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知化学反应①:Fe(s)+CO2(g) ![]() FeO(s)+CO(g),其平衡常数为K1;化 反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其平衡常数为K1;化 反应②:Fe(s)+H2O(g) ![]() FeO(s)+H2(g),其平衡常数为K2,在温度973 K和1173 K情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其平衡常数为K2,在温度973 K和1173 K情况下,K1、K2的值分别如下:
温度 | K1 | K2 |
973 K | 1.47 | 2.38 |
1173 K | 2.15 | 1.67 |
请填空:(1)通过表格中的数值可以推断:K1随温度的升高而____________,(填增大,减小,不变),所以反应①是____________(填“吸热”或“放热”)反应。
(2)现有反应③:CO2(g)+H2(g) ![]() CO(g)+H2O(g),请你写出该反应的平衡常数K3的数表达式:K3=__________,根据数据可知反应③是吸热反应。
CO(g)+H2O(g),请你写出该反应的平衡常数K3的数表达式:K3=__________,根据数据可知反应③是吸热反应。
(3)要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有___(填写字母序号,下同)。
A.增大压强(压缩容器体积)
B.体积不变时充入稀有气体
C.升高温度
D.使用合适的催化剂
(4)图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:

①图甲中t2时刻发生改变的条件可能是_____________ 、____________。
②图乙中t2时刻发生改变的条件可能是__________。
A.升高温度 B.降低温度 C.加入催化剂 D.增大压强 E.减小压强 F.充入CO2 G.分离出部分CO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可与其最高价含氧酸反应生成离子化合物,由此可知

A. X、Y、Z中最简单氢化物稳定性最弱的是Y
B. Z元素氧化物对应水化物的酸性一定强于Y
C. X元素形成的单核阴离子还原性大于Y
D. Z元素单质在化学反应中只表现氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用金属活动性的不同,可以采取不同的冶炼方法冶炼金属。下列反应所描述的冶炼方法不可能实现的是( )
A. 2Al2O3(熔融)![]() 4Al+3O2↑
4Al+3O2↑
B. Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
C. Fe+CuSO4 =FeSO4+Cu
D. 2NaCl(水溶液)![]() 2Na+Cl2↑
2Na+Cl2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将AgCl分别加入盛有:①5 mL水;② 6 mL0.5mol·L-1 NaCl溶液;③10 mL0.2mol·L-1 CaCl2溶液;④50 mL0.1mol·L-1盐酸的烧杯中,均有固体剩余,各溶液中c(Ag+)从大到小的顺序排列正确的是
A. ④③②① B. ②③④① C. ①④③② D. ①③②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在氢氟酸溶液中,存在如下电离平衡:HF![]() H+ + F-
H+ + F-
(1)加入固体NaOH ,电离平衡向________移动, c(H+)_______________。
(2)加入固体NaF , 电离平衡向________移动 , c(H+)____________。
(3)常温下,pH=12的NaOH和pH= 2的HCl等体积混合后,pH= ____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图的转化关系判断下列说法正确的是(反应条件已略去)
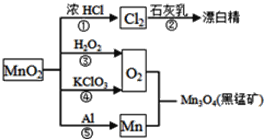
A. 反应⑤说明该条件下铝的还原性强于锰
B. 反应①②③④⑤均属于氧化反应和离子反应
C. 相同条件下生成等量的O2,反应③和④转移的电子数之比为1∶1
D. 反应①中氧化剂与还原剂的物质的量之比为1∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究![]() 的性质,某同学按如图所示的装置进行实验。
的性质,某同学按如图所示的装置进行实验。

完成下列填空:
(1)装置A中盛放浓碱酸的仪器名称是________________,A中发生反应的化学方程式是___________________。
(2)装置B中的现象是________________________,说明![]() 具有________(填代码);装置C中发生反应的化学方程式是________________________________,说明
具有________(填代码);装置C中发生反应的化学方程式是________________________________,说明![]() 具有________(填代码)。
具有________(填代码)。
a.氧化性 b.还原性 c.漂白性 d.酸性
(3)装置D的目的是探究![]() 与品红作用的可逆性,写出实验操作及现象________________________尾气可采用________溶液吸收。
与品红作用的可逆性,写出实验操作及现象________________________尾气可采用________溶液吸收。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对污水处理的化学方法及其原理的描述错误的是( )
A. 明矾放入污水中就会发生反应: Al3++3H2O![]() Al(OH)3(胶体)+3H+
Al(OH)3(胶体)+3H+
B. 用氢氧化钙来中和钢铁厂、电镀厂产生的酸性废水,用硫酸或CO2中和碱性废水
C. 利用沉淀反应是除去水中重金属离子常用的方法
D. 处理含有重金属离子的废水一定不涉及氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com