
【题目】二氧化硫能够使品红溶液褪色,表现了二氧化硫的( )
A. 氧化性 B. 还原性 C. 漂白性 D. 酸性氧化物的性质
 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:
【题目】用下列仪器的编号回答问题:
①容量瓶 ②蒸馏烧瓶 ③量筒④烧杯 ⑤托盘天平⑥分液漏斗
(1)加热时必须垫石棉网的有_______________,
(2)使用时必须检查是否漏水的有____________,
(3)标有零刻度的有________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1molCH3OH(甲醇)和1molH2混合气体和足量的氧气燃烧后,在150℃时 将混合气体通过足量的Na2O2后,Na2O2增重的质量为
A. 15g B. 34g C. 60g D. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】偏钒酸铵(NH4VO3)主要用作催化剂、催干剂、媒染剂等.用沉淀法除去工业级偏钒酸铵中的杂质硅、磷的流程如图1: 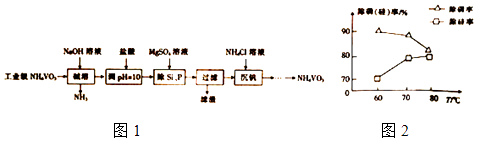
(1)碱溶时,下列措施有利于NH3逸出的是(填字母). a、升高温度 b、增大压吸 c、增大NaOH溶液的浓度
(2)①滤渣的主要成分为Mg3(PO4)2、MgSiO3 , 已知Ksp(MgSiO3)=2.4×l0﹣5 . 若滤液中c(SiO32﹣)=0.08mol/L,则c(Mg2+)= ②由图2可知,加入一定量的MgSO4溶液作沉淀剂时,随着温度的升高,除磷率下降,其原因是温度升高,Mg3(PO4)2溶解度增大和;但随着温度的升高,除硅率升高,其原因是(用离子方程式表示).
(3)沉钒时,反应温度需控制在50℃,在实验室可采取的加热方式为
(4)探究NH4Cl的浓度对沉钒率的影响,设计实验步骤(常见试剂任选):取两份10mL一定浓度的滤液A和B,分别加入lmL和10mL的1mol/LNH4Cl溶液,再向A中加入mL蒸馏水,控制两份溶液温度均为50℃、pH均为8,由专用仪器洲定沉钒率.加入蒸馏水的目的是
(5)偏钒酸铵本身在水中的溶解度不大,但在草酸(H2C2O4)溶液中因发生氧化还原反应而溶解,同时生成络合物(NH4)2[(VO)2(C2O4)3],该反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇脱氢可制取甲醛:CH3OH(g)HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示(已知反应在1L的密闭容器中进行、甲醇的物质的量为1mol).下列有关说法中正确的是( ) 
A.脱氢反应的△H<0
B.600 K时,Y点甲醇的v(逆)<v(正)
C.从Y点到Z点可通过增大压强
D.在t1K时,该反应的平衡常数为8.1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某致病细菌分泌的外毒素为无色、细针状结晶,对小鼠和人体有很强的毒性,可引起流涎、呕吐、便血、痉挛等,最终导致死亡。该外毒素为环状肽,结构式如图所示。

请据图分析回答下面的问题。
(1)该化合物中含有________个游离的氨基,________个游离的羧基。
(2)组成该化合物的氨基酸有_______种,其中重复出现的R基是_______________,请写出氨基酸的结构通式:____________________________。
(3)该化合物含有________个肽键。
(4)b框所示的R基所构成的氨基酸的相对分子质量是________。
(5)该外毒素在环状肽形成过程中失去了________个水分子,相对分子质量减少了________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能获得成功的是( )
A.用溴水可鉴别苯、CCl4、己烯
B.加浓溴水,然后过滤可除去苯中少量己烯
C.苯、溴水、铁粉混合制成溴苯
D.可用分液漏斗分离己烷和苯的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇脱氢可制取甲醛:CH3OH(g)HCHO(g)+H2(g),甲醇的平衡转化率随温度变化曲线如图所示(已知反应在1L的密闭容器中进行、甲醇的物质的量为1mol).下列有关说法中正确的是( ) 
A.脱氢反应的△H<0
B.600 K时,Y点甲醇的v(逆)<v(正)
C.从Y点到Z点可通过增大压强
D.在t1K时,该反应的平衡常数为8.1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物与生产、生活关系密切.t℃时,反应FeO(s)+CO(g)Fe(s)+CO2(g)的平衡常数K=0.25,反应达到平衡时n(CO):n(CO2)= . 若在1L密闭容器中加入0.02mol FeO(s),并通入xmolCO,t℃时反应达到平衡.此时FeO(s)转化率为50%,则x= .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com