
【题目】钠硫电池作为一种新型储能电池,其应用逐渐得到重视和发展。
(1)钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2SX)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,其反应原理如下图所示:
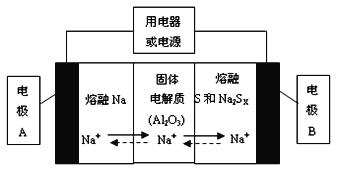
①根据上右表数据,请你判断该电池工作的适宜应控制在_________(填字母)范围内。
物质 | Na | S | Al2O3 |
熔点/℃ | 97.8 | 115 | 2050 |
沸点/℃ | 892 | 444.6 | 2980 |
a.100℃以下 b.100~300℃ c.300~350℃ d.350~2050℃
②放电时,电极A为_________极,电极B发生_________反应(填“氧化或还原”)
③充电时,总反应为Na2SX=2Na+xS(3<x<5),则阳极的电极反应式为:________________。
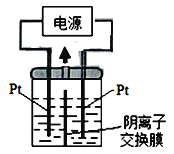
(2)若把钠硫电池作为电源,电解槽内装有KI及淀粉溶液如图所示,槽内的中间用阴离子交换膜隔开。通电一段时间后,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。则右侧发生的电极方程式:___________;试分析左侧溶液蓝色逐渐变浅的可能原因是:___________。
(3)若把钠硫电池作为电源,按如图所示装置进行实验电解乙池和丙池:
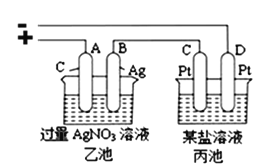
当钠硫电池中消耗0.05xmol的S时,理论上乙池中B极的质量增加__________g;此时丙装置中___________(填“C”或“D”)电极析出7.20g金属,则丙装置中的某盐溶液可能是_______(填序号)。
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
【答案】C 负 还原 SX2--2e-=xS 2H2O+2e—=H2↑+2OH—(2H++2e—=H2↑) 右侧溶液中生成的OH—通过阴离子交换膜进入左侧溶液,并与左侧溶液中I2反应等 10.8 D bd
【解析】
(1)原电池工作时,控制的温度应为满足Na、S为熔融状态,Na被氧化,应为原电池负极,阳离子向正极移动,充电时,阳极反应为原电池正极反应的逆反应,应生成S,以此解答;
(2)左侧溶液变蓝色,生成I2,左侧电极为阳极,电极反应为:2I--2e-=I2,右侧电极为阴极,电极反应式为:2H2O+2e-=H2↑+2OH-,右侧放出氢气,右侧I-、OH-通过阴离子交换膜向左侧移动,发生反应3I2+6OH-=IO3-+5I-+3H2O,一段时间后,蓝色变浅,保证两边溶液呈电中性,左侧的IO3-通过阴离子交换膜向右侧移动,由此分析解答。
(3)根据串联电路中电子转移数相等,结合电化学的工作原理分析作答。
(1)①原电池工作时,控制的温度应为满足Na、S为熔融状态,则温度应高于115℃而低于444.6℃,只有C符合,
故答案为:C;
②放电时,Na被氧化,则A应为原电池负极,B为正极发生还原反应,故答案为:负;还原;
③充电时,是电解池反应,阳极反应为:SX2--2e-=xS;
(2)根据以上分析,左侧溶液变蓝色,生成I2,左侧电极为阳极,电极反应为:2I2e=I2,右侧电极为阴极,电极反应式为:2H2O+2e—=H2↑+2OH-(2H++2e-=H2↑),右侧I、OH通过阴离子交换膜向左侧移动,发生反应3I2+6OH=IO3+5I+3H2O,一段时间后,蓝色变浅,故答案为:2H2O+2e—=H2↑+2OH-(2H++2e-=H2↑);右侧溶液中生成的OH-通过阴离子交换膜进入左侧溶液,并与左侧溶液中I2反应等;
(3)根据反应式SX2--2e-=xS可知,当钠硫电池中消耗0.05xmol的S时,电子转移数为0.1mol,则乙池是电解池,B极上银离子得电子发生还原反应而析出银,根据转移电子数相等,乙池中B极的质量增加0.1mol![]() 108g/mol=10.8g;丙池是电解池,阴极上金属离子放电析出金属单质,D连接电源的负极,则D是阴极,电极质量会增加;根据转移电子相等知,当析出金属时,则该金属元素在氢元素之后,ac项错误,bd正确,故答案为:bd。
108g/mol=10.8g;丙池是电解池,阴极上金属离子放电析出金属单质,D连接电源的负极,则D是阴极,电极质量会增加;根据转移电子相等知,当析出金属时,则该金属元素在氢元素之后,ac项错误,bd正确,故答案为:bd。


科目:高中化学 来源: 题型:
【题目】为达到下表中的实验目的,请选择合适的试剂和方法.
实验目的 | 试剂及方法 |
①除去碳酸钠粉末中混入的碳酸氢钠杂质 | _____ |
②鉴别Na2SO4溶液和(NH4)2SO4溶液 | _____ |
③除去SiO2中的Fe2O3 | _____ |
④除去FeCl2溶液中少量的FeCl3 | _____ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用光伏电池提供电能处理废水中的污染物(有机酸阴离子用R-表示),并回收有机酸HR,装置如图所示。下列说法错误的是
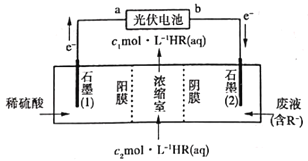
A.在光伏电池中a极为正极B.石墨(2)极附近溶液的pH降低
C.HR溶液:c2<c1D.若两极共收集3mol气体,则理论上转移4mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电—Fenton法是用于水体里有机污染物降解的高级氧化技术,其反应原理如图所示,其中电解产生的H2O2与Fe2+发生Fenton反应,Fe2++H2O2=Fe3++OH-+OH,生成的烃基自由基(OH)能氧化降解有机污染物。下列说法正确的是( )
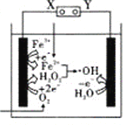
A. 电解池左边电极的电势比右边电极的电势高
B. 电解池中只有O2和Fe3+发生还原反应
C. 消耗1 molO2,电解池右边电极产生4mol OH
D. 电解池工作时,右边电极附近溶液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一镁铝合金共51 g,把其加入到1 L 5 mol·L-1的盐酸中,恰好反应完。
(1)关于合金的下列说法正确的有________。
A.合金只能由两种或两种以上的金属组成
B.合金的硬度一般比其组成成分金属的硬度大
C.镁铝熔成合金的过程是一个化学过程
D.合金的熔点一般比其组成成分的熔点低
E.合金具备金属的特性
(2) 该合金中镁铝的质量分别为________g、________g。
(3) 反应中共收集到标况下的氢气的体积为___________L。
(4)向反应后的溶液中逐滴加入5 mol·L-1的NaOH溶液,若要使沉淀恰好达到最大值,需要加入NaOH________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有4种钠的化合物W、X、Y、Z,它们之间存在如下关系:
①W![]() X+H2O+CO2↑
X+H2O+CO2↑
②Z+CO2→X+O2
③Z+H2O→Y+O2↑
④X+Ca(OH)2→Y+CaCO3↓
试回答下列问题:
(1) W、X、Y、Z的化学式分别是:W:________,X:________,Y:________,Z:________。
(2)以上4个化学反应,属于氧化还原反应的是________(填反应序号),反应中氧化剂是________(写化学式)。
(3)若④反应在溶液中进行,写出其离子方程式以及能用该离子方程式表示的另一个化学反应的化学方程式:
①离子方程式:______________________________________________。
②化学方程式:________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某组甲乙同学进行稀硫酸与锌制取氢气的实验,请回答下列问题:
(1)甲同学发现加入少量硫酸铜溶液可加快氢气的生成速率。为了进一步研究硫酸铜的量对氢气生成速率的影响,设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
实验 混合溶液 | A | B | C | D | E | F |
4 mol·L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1=___,V6=___,V9=___;
②反应一段时间后,实验A中的金属呈___色,实验E中的金属呈___色;
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因___________________________。
(2)乙同学为了探究锌与稀硫酸反应过程中的速率及能量的变化,进行以下实验,分析影响反应速率的因素。
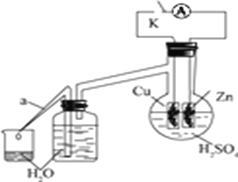
实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1分钟内从a管流出的水滴数,得到的水滴数如下表所示:
1分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
1分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
分析反应过程中的水滴数,请回答:
① 由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率快,主要原因是__________________________________________________________。
② 由水滴数102>78,说明在反应后期,断开K时的反应速率快于闭合K时的反应速率,主要原因是____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究硫酸亚铁的分解产物,将硫酸亚铁装入下图所示的装置a中,打开K1和K2缓缓通入N2加热。实验后反应管中残留固体为红色粉末。下列说法中正确的是
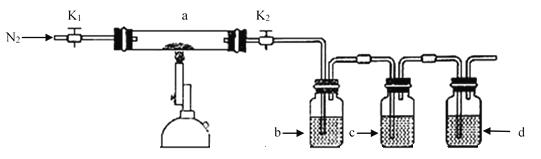
A.分解的气体产物中有SO3、SO2应该先检验SO3
B.装置b中的试剂为Ba(NO3)2溶液,反应后有白色沉淀生成,证明分解产物中有SO3气体
C.装置c中的试剂为酸性KMnO4溶液,作用是除去混合气体中的SO2
D.装置d之后需要增加尾气处理装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等物质的量的X(g)与Y(g)在密闭容器中进行可逆反应:X(g)+Y(g) ![]() 2Z(g)+W(s) ΔH<0,下列叙述正确的是 ( )
2Z(g)+W(s) ΔH<0,下列叙述正确的是 ( )
A. 平衡常数K值越大,X的转化率越大
B. 达到平衡时,反应速率v正(X)=2v逆(Z)
C. 达到平衡后降低温度,正向反应速率减小的倍数大于逆向反应速率减小的倍数
D. 达到平衡后,升高温度或增大压强都有利于该反应平衡向逆反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com