
 某化学实验室需要0.2mol/L NaOH溶液500mL和0.5mol/L硫酸溶液450mL.根据这两种溶液的配制情况回答下列问题:
某化学实验室需要0.2mol/L NaOH溶液500mL和0.5mol/L硫酸溶液450mL.根据这两种溶液的配制情况回答下列问题:| 1000ρw |
| M |
| n |
| V |
| 1000×1.84×98% |
| 98 |
| 0.5mol/L×0.5L |
| 18.4mol/L |
| n |
| V |
| n |
| V |
| n |
| V |
| n |
| V |
| n |
| V |


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源: 题型:
 25℃时,在20mL 0.1mol/L NaOH溶液中加入0.2mol/L CH3COOH溶液,所加入溶液的体积(v)和混合液中pH变化关系的曲线如图所示,若B点的横坐标a=10,下列分析的结论正确的是( )
25℃时,在20mL 0.1mol/L NaOH溶液中加入0.2mol/L CH3COOH溶液,所加入溶液的体积(v)和混合液中pH变化关系的曲线如图所示,若B点的横坐标a=10,下列分析的结论正确的是( )| A、在B点有:c(Na+)=c(CH3COO-) |
| B、对曲线上A、B间任何一点,溶液中都有:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| C、C点时,c(CH3COO-)=c(Na+)>c(H+)=c(OH-) |
| D、D点时,c(CH3COO-)+c(CH3COOH)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①和③ | B、只有② |
| C、只有③ | D、①和④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

 制备比
制备比 少2个氢原子的芳香烃的合成路线
少2个氢原子的芳香烃的合成路线| 浓硫酸 |
| 170℃ |
| Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 醇 |
| 醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:
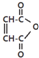 是一种有机试剂和有机合成原料,是丁烯二酸的酸酐.欲由1,3-丁二烯为原料制取丁烯二酸(HOOCCH=CHCOOH),设计如下四种路径(其中“氧化”指用强氧化剂将醇羟基氧化为羧基).
是一种有机试剂和有机合成原料,是丁烯二酸的酸酐.欲由1,3-丁二烯为原料制取丁烯二酸(HOOCCH=CHCOOH),设计如下四种路径(其中“氧化”指用强氧化剂将醇羟基氧化为羧基).查看答案和解析>>
科目:高中化学 来源: 题型:
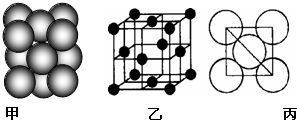
 X、Y、Z、W为短周期的主族元素,其原子序数依次增大.X元素形成的单质是自然界中含量最多的气体.Y是电负性最大的元素.W的原子最外层电子数与核外电子总数之比为3:8.X的原子序数是Z的原子序数的一半.U原子基态的外围电子排布3d104s1.
X、Y、Z、W为短周期的主族元素,其原子序数依次增大.X元素形成的单质是自然界中含量最多的气体.Y是电负性最大的元素.W的原子最外层电子数与核外电子总数之比为3:8.X的原子序数是Z的原子序数的一半.U原子基态的外围电子排布3d104s1.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、O4是氧元素的一种同位素 |
| B、O4可能含有极性键 |
| C、同温同压下,等体积的O4气体和O2含有相同的分子数 |
| D、O4转化O2为物理变化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com