
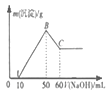
ЎҫМвДҝЎҝДіИЬТәЦРә¬УРH+ЎўMg2+ЎўAl3+ИэЦЦСфАлЧУЈ¬ЦрөОјУИл1mol/LNaOHИЬТәЈ¬ПыәДNaOHИЬТәМе»эәНЙъіЙіБөнЦ®јдөД№ШПөИзНјЛщКҫЈ¬ФтПВБРЛө·ЁХэИ·өДКЗЈЁ Ј©
A.әбЧшұк0-50mLКұЈ¬·ўЙъ·ҙУҰЦ»УРЈәMg2++2OH-ЁTMg(OH)2ЎэЈ¬Al3++3OH-ЁTAl(OH)3Ўэ
B.BөгЙъіЙіБөнөДОпЦКөДБҝОӘ0.02mol
C.ИфНщCөгөДИЬТәЦРјУИл0.1mol/LСОЛб50mLЈ¬іБөнҪ«И«ІҝИЬҪв
D.H+ЎўMg2+ЎўAl3+ИэЦЦСфАлЧУОпЦКөДБҝЕЁ¶ИЦ®ұИОӘ2Јә1Јә2
Ўҫҙр°ёЎҝD
ЎҫҪвОцЎҝ
ёщҫЭНјПуҝЙЦӘЈ¬әбЧшұкОӘ0-10mLКұ·ўЙъөД·ҙУҰОӘH++OH-=H2OЈ¬јУИл10mLNaOHИЬТәЦРәНH+Ј¬УЙn(H+)=n(NaOH)Ј»10-50mLКұ·ўЙъөД·ҙУҰОӘMg2++2OH-ЁTMg(OH)2ЎэЎўAl3++3OH-ЁTAl(OH)3ЎэЈ¬іБөнОӘЧоҙуЦөКұЈ¬ёГҪЧ¶ОПыәД40mL NaOHИЬТәЈ¬ёщҫЭOH-КШәгҝЙөГЈә2n[Mg(OH)2]+3n[Al(OH)3]=n(NaOH)Ј¬ҪбәПMgКШәгөГn(Mg2+)=n[Mg(OH)2]Ј¬50-60mLКұЈ¬·ўЙъөД·ҙУҰОӘAl(OH)3+OH-=AlO2-+2H2OЈ¬Al(OH)3НкИ«ИЬҪвПыәД10mL NaOHИЬТәЈ¬ёщҫЭПыәДөДЗвСх»ҜДЖјЖЛгn[Al(OH)3]Ј¬ФЩёщҫЭВБКШәгЦӘn(Al3+)=n[Al(OH)3]Ј¬ҫЭҙЛјЖЛгЎЈ
A. әбЧшұк0-50mLКұЈ¬·ўЙъ·ҙУҰУРЈәH++OH-=H2OЎўMg2++2OH-ЁTMg(OH)2ЎэЈ¬Al3++3OH-ЁTAl(OH)3ЎэЈ¬AПоҙнОуЈ»
B. ёщҫЭНјПуҝЙЦӘЈ¬әбЧшұкОӘ0-10mLКұ·ўЙъөД·ҙУҰОӘH++OH-=H2OЈ¬јУИл10mLNaOHИЬТәЦРәНH+Ј¬УЙn(H+)=n(NaOH)=0.01LЎБ1mol/L=0.01molЈ¬50-60mLКұЈ¬·ўЙъөД·ҙУҰОӘAl(OH)3+OH-=AlO2-+2H2OЈ¬Al(OH)3НкИ«ИЬҪвПыәД10mL NaOHИЬТәЈ¬УЙ·ҪіМКҪҝЙЦӘn[Al(OH)3]=n(NaOH)=0.01LЎБ1mol/L=0.01molЈ¬ёщҫЭВБКШәгЦӘn(Al3+)=n[Al(OH)3]= 0.01molЈ¬10-50mLКұ·ўЙъөД·ҙУҰОӘMg2++2OH-ЁTMg(OH)2ЎэЎўAl3++3OH-ЁTAl(OH)3ЎэЈ¬іБөнОӘЧоҙуЦөКұЈ¬ёГҪЧ¶ОПыәД40mL NaOHИЬТәЈ¬ёщҫЭOH-КШәгҝЙөГЈә2n[Mg(OH)2]+3n[Al(OH)3]=n(NaOH)Ј¬ТтҙЛ2n[Mg(OH)2]+0.03mol=0.04LЎБ1mol/LЈ¬ҝЙөГn[Mg(OH)2]=0.005molЈ¬ТтҙЛBөгЙъіЙіБөнөДОпЦКөДБҝОӘ0.01mol+0.005mol=0.015molЈ¬BПоҙнОуЈ»
C. CөгИЬТәЦРөДіБөнОӘMg(OH)2Ј¬ЖдОпЦКөДБҝОӘ0.005molЈ¬ТӘИГіБөнНкИ«ИЬҪвЈ¬РиТӘСОЛбөДОпЦКөДБҝОӘ0.01molЈ¬јУИл0.1mol/LСОЛбөДМе»эОӘ![]() =0.1L=100mLЈ¬CПоҙнОуЈ»
=0.1L=100mLЈ¬CПоҙнОуЈ»
D. ИЬТәЦРH+ЎўMg2+ЎўAl3+ИэЦЦСфАлЧУОпЦКөДБҝЕЁ¶ИЦ®ұИОӘ0.01:0.005:0.01=2:1:2Ј¬DПоХэИ·Ј»
ҙр°ёСЎDЎЈ



| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝТСЦӘІҝ·Цұ»Сх»ҜөДГҫМх1Ј®6 gЈ¬әНЧгБҝөДСОЛб·ҙУҰЈ¬ФЪұкЧјЧҙҝцПВЙъіЙH21Ј®12 LЈ¬ФЪёъСОЛб·ҙУҰЗ°ұ»Сх»ҜөДГҫКЗ ( )
A.1Ј®2 gB.0Ј®64 gC.0Ј®4 gD.0Ј®24 g
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ¶МЦЬЖЪЦчЧеФӘЛШWЎўXЎўYЎўZөДФӯЧУРтКэТАҙОФцҙуЈ¬XКЗҪрКфФӘЛШЈ¬WЎўYКЗІ»Н¬ЦчЧеөД·ЗҪрКфФӘЛШЗТЧоНвІгөзЧУКэОӘЕјКэЈ¬YөДФӯЧУРтКэКЗZөДЧоНвІгөзЧУКэөД2ұ¶Ј¬УЙWЎўXЎўYИэЦЦФӘЛШРОіЙөД»ҜәПОпMөДҪб№№ИзПВНјЛщКҫЎЈПВБРРрКцХэИ·өДКЗ
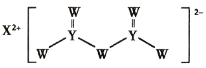
A.WЎўXАлЧУ°лҫ¶ұИҪПЈәX>W
B.YЎўZөДЗв»ҜОпОИ¶ЁРФұИҪПЈәY>Z
C.1mol YW2ҫ§МеЦРә¬УР4mol YЎӘWјь
D.№ӨТөЙПҝЙНЁ№эөзҪвИЫИЪXWАҙЙъІъXөДөҘЦК
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝ25ЎжКұЈ¬H3AsO4Л®ИЬТәЦРә¬ЙйөДёчОпЦЦөД·ЦІј·ЦКэ(ЖҪәвКұДіОпЦЦөДЕЁ¶ИХјёчОпЦЦЕЁ¶ИЦ®әНөД·ЦКэ)УлpHөД№ШПө·ЦұрИзНјЛщКҫЎЈ
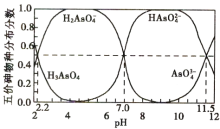
ПВБРРрКцҙнОуөДКЗ
A.Ҫ«NaOHИЬТәЦрөОјУИлөҪH3AsO4ИЬТәЦРЈ¬өұИЬТәpHФЪ5Ў«6Кұ·ўЙъ·ҙУҰөДАлЧУ·ҪіМКҪОӘ![]()
B.Na2HAsO4ИЬТәЦРАлЧУЕЁ¶И№ШПөc(Na+)Јҫc(HAsO![]() )Јҫc(OHЈӯ)Јҫc(H2AsO
)Јҫc(OHЈӯ)Јҫc(H2AsO![]() )Јҫc(AsO
)Јҫc(AsO![]() )
)
C.ПтH3AsO4ИЬТәөОјУNaOHИЬТәЦБЦРРФКұc(Na+)=2c(HAsO![]() )+3c(AsO
)+3c(AsO![]() )
)
D.AsO43-өЪТ»ІҪЛ®ҪвөДЖҪәвіЈКэөДКэБҝј¶ОӘ10Јӯ3
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝБЧЛбВИаӯ(Ҫб№№ИзНјЛщКҫ)ФЪПё°ыЛ®ЖҪЙПДЬУРР§ТЦЦЖРВРН№ЪЧҙІЎ¶ҫөДёРИҫЈ¬ОТ№ъУЎ·ўөДЎ¶РВРН№ЪЧҙІЎ¶ҫ·ОСЧХпБЖ·Ҫ°ё(КФРРөЪЖЯ°ж)Ў·ЦРГчИ·№ж¶ЁБЛЖдУГБҝЎЈ
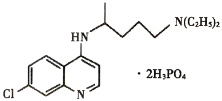
(1)МјЎў№иЎўХаОӘН¬Т»ЦчЧеФӘЛШЈ¬Фт»щМ¬№иФӯЧУәЛНвөзЧУөДҝХјдФЛ¶ҜЧҙМ¬УР________ЦЦЈ¬»щМ¬ХаФӯЧУөДЧоНвІгөДөзЧУЕЕІјНјОӘ__________________ЎЈ
(2)CЎўNЎўOИэЦЦФӘЛШөЪТ»өзАлДЬУЙҙуөҪРЎөДЛіРтКЗ_____________________ЎЈ
(3)БЧЛбВИаӯ·ЦЧУЦРөӘФӯЧУөДФУ»Ҝ·ҪКҪОӘ________Ј¬ұҪ»·ЦРә¬УРөД№ІјЫјьАаРНКЗ________ЎЈ
(4)![]() өДҝХјд№№РНКЗ____________Ј¬Ул
өДҝХјд№№РНКЗ____________Ј¬Ул![]() »ҘОӘөИөзЧУМеөД·ЦЧУКЗ____________(РҙТ»ЦЦјҙҝЙ)ЎЈ
»ҘОӘөИөзЧУМеөД·ЦЧУКЗ____________(РҙТ»ЦЦјҙҝЙ)ЎЈ
(5)УЙCЎўHЎўOФӘЛШЧйіЙөДH2OәНC2H5OHҝЙТФИОТвұИАэ»ҘИЬЈ¬ЖдФӯТтКЗ________________ЎЈ
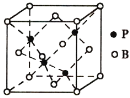
(6)УЙPУлBФӘЛШРОіЙөД»ҜәПОпBPөДҫ§°ы(ИзНјЛщКҫ)ЦРBІЙУГГжРДБў·Ҫ¶С»эЈ¬PФӯЧУМоИлЛДГжМеҝХП¶ЦРЎЈТСЦӘҫ§°ыұЯіӨОӘa pmЈ¬ҫ§МеЦРBФӯЧУУлPФӯЧУөДЧоҪьҫаАлКЗ___________Ј¬Йи°ў·ьјУөВВЮіЈКэөДЦөОӘNAЈ¬ФтBPҫ§МеөДГЬ¶ИКЗ___________gЈҜcm3(БРіцјЖЛгұнҙпКҪ)ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝҪ«3molAәН1molB»мәПУЪТ»Ме»эҝЙұдөДГЬұХИЭЖчPЦРЈ¬ТФҙЛКұөДОВ¶ИЎўС№ЗҝәНМе»эЧчОӘЖрКјМхјюЈ¬·ўЙъИзПВ·ҙУҰЈә3A(g)Ј«B(g)![]() 2C(g)Ј«D(g)Ј¬ҙпөҪЖҪәвКұCөДЕЁ¶ИОӘwmol/LЎЈ»ШҙрПВБРОКМвЈә
2C(g)Ј«D(g)Ј¬ҙпөҪЖҪәвКұCөДЕЁ¶ИОӘwmol/LЎЈ»ШҙрПВБРОКМвЈә
ЈЁ1Ј©ұЈіЦОВ¶ИәНС№ЗҝІ»ұдЈ¬°ҙПВБРЛДЦЦЕдұИідИлИЭЖчPЦРУР№ШОпЦКЈ¬ЖҪәвәуCөДЕЁ¶ИИФОӘwmol/LөДКЗ___ЎЈ
AЈ®6molAЈ«2 molB BЈ®3molAЈ«1molBЈ«2molC
CЈ®2molCЈ«1molBЈ«1molD DЈ®1molCЈ«2molD
ЈЁ2Ј©ұЈіЦФӯЖрКјОВ¶ИәНМе»эІ»ұдЈ¬ТӘК№ЖҪәвәуCөДЕЁ¶ИИФОӘwmol/LЈ¬УҰ°ҙПВБРДДЦЦЕдұИПтИЭЖчQЦРідИлУР№ШОпЦК___ЎЈ
AЈ®3molAЈ«1 molB
BЈ®4molCЈ«2molD
CЈ®1.5molAЈ«0.5molBЈ«1molCЈ«0.5molD
DЈ®ОЮ·ЁЕР¶П
ЈЁ3Ј©ұЈіЦФӯЖрКјОВ¶ИәНМе»эІ»ұдЈ¬ИфИФ°ҙ3molAәН1molBЕдұИФЪИЭЖчQЦР·ўЙъ·ҙУҰЈ¬ФтЖҪәвКұCөДЕЁ¶ИәНwmol/LөД№ШПөКЗ___ЎЈ
AЈ®ҙуУЪwmol/L BЈ®РЎУЪwmol/L CЈ®өИУЪwmol/L DЈ®ОЮ·ЁұИҪП
ЈЁ4Ј©Ҫ«2molCәН2molD°ҙЖрКјОВ¶ИәНС№ЗҝідИлИЭЖчQЦРЈ¬ұЈіЦОВ¶ИәНМе»эІ»ұдЈ¬ЖҪәвКұCөДЕЁ¶ИОӘvmol/LЈ¬ФтvәНwөД№ШПөКЗ___ЎЈ
AЈ®v>w BЈ®v<w CЈ®vЈҪw DЈ®ОЮ·ЁұИҪП
ЈЁ5Ј©Ҫ«МвёЙЦРөДМе»эҝЙұдөДГЬұХИЭЖчPёДОӘәгИЭМхјюЈ¬ФЪДіОВ¶ИПВЈ¬Ҫ«2.4molAәН0.8molB»мәПУЪёГИЭЖчЦР·ўЙъЙПКц·ҙУҰЈ¬ҙпөҪЖҪәвКұCөДОпЦКөДБҝОӘnmolЎЈИфAЎўBЎўCЎўDЖрКјөДОпЦКөДБҝ·ЦұрУГaЎўbЎўcЎўdұнКҫЈ¬ұЈіЦәгОВәгИЭЈ¬ТӘК№·ҙУҰҝӘКјКұПтДж·ҙУҰҪшРРЈ¬ЗТҙпөҪЖҪәвәуCөДОпЦКөДБҝИФОӘn molЈ¬ФтЖрКјКұCөДОпЦКөДБҝИЎЦө·¶О§КЗ___ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝClO2КЗТ»ЦЦЙұҫъПы¶ҫР§ВКёЯЎў¶юҙООЫИҫРЎөДЛ®ҙҰАнјБЎЈКөСйКТЦРҝЙНЁ№эТФПВ·ҙУҰЦЖөГЈә2KClO3Ј«H2C2O4Ј«H2SO4![]() 2ClO2ЎьЈ«K2SO4Ј«2CO2ЎьЈ«2H2OЎЈПВБРЛө·ЁІ»ХэИ·өДКЗЈЁ Ј©
2ClO2ЎьЈ«K2SO4Ј«2CO2ЎьЈ«2H2OЎЈПВБРЛө·ЁІ»ХэИ·өДКЗЈЁ Ј©
AЈ®CO2КЗСх»ҜІъОп
BЈ®H2C2O4ФЪ·ҙУҰЦРұ»Сх»Ҝ
CЈ®H2C2O4өДСх»ҜРФЗҝУЪClO2өДСх»ҜРФ
DЈ®ClO2ЧчЛ®ҙҰАнјБКұЈ¬АыУГБЛЖдЗҝСх»ҜРФ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝУГјоРФЗвСхИјБПөзіШОӘөзФҙҪшРРөзҪвөДКөСйЧ°ЦГКҫТвНјИзНјЛщКҫЎЈПВБРЛө·ЁЦРХэИ·өДКЗЈЁ Ј©

A.ИјБПөзіШ№ӨЧчКұёәј«·ҙУҰОӘЈәH2=2H++2e-
B.ИфТӘКөПЦМъЙП¶ЖНӯЈ¬Фтaј«КЗМъЈ¬bј«КЗНӯ
C.ИфТӘКөПЦөзҪвҫ«Б¶ҙЦНӯЈ¬Фтaј«·ўЙъСх»Ҝ·ҙУҰЈ¬bј«ЙПУРНӯОціц
D.aЎўbБҪј«ҫщКЗКҜД«КұЈ¬ФЪПаН¬МхјюПВЈ¬өұөзіШЦРПыәДH222.4LЈЁұкЧјЧҙҝцЈ©КұЈ¬aј«ОціцНӯ64g
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝОӘБЛіэИҘCuCl2ЛбРФИЬТәЦРөДFeCl3,јУИИҪБ°иөДМхјюПВјУИлТ»ЦЦКФјБЈ¬И»әуФЩјУИлККБҝСОЛбЈ¬ёГКФјБІ»ДЬКЗ(ЎЎЎЎ)
A.Cu(OH)2B.CuCO3C.NaOHD.CuO
Ійҝҙҙр°ёәНҪвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com