
【题目】实验室需要配制0.1 mol·L-1CuSO4溶液480 mL。按下列操作步骤填上适当的文字,以使整个操作完整。
(1)选择仪器。完成本实验所必需的仪器有:托盘天平(精确到0.1 g)、药匙、烧杯、量筒、玻璃棒、________、________以及等质量的两片滤纸。
(2)计算,应选择下列________。
A.需要CuSO4固体8 g B.需要CuSO4固体7.7 g
C.需要CuSO4·5H2O晶体12.5 g D.需要CuSO4·5H2O晶体12.0 g
(3)称量。所用砝码生锈则所配溶液的浓度会_____(填“偏高”“偏低”或“无影响”。
(4)溶解、冷却,该步实验中需要使用玻璃棒,目的是____________________。
(5)转移、洗涤。在转移时应使用________引流,需要洗涤烧杯2~3次是为了________。
(6)定容,摇匀。
(7)将配好的溶液静置一段时间后,倒入指定的试剂瓶,贴好标签,注明配制的时间、溶液名称及浓度。
(8)在配制过程中,某学生观察定容时液面情况如图所示,所配溶液的浓度会________(填“偏高”“偏低”或“无影响”)。

【答案】胶头滴管 500mL容量瓶A C偏高搅拌、加速溶解玻璃棒防止溶质损失(或保证溶质不损失)偏低
【解析】
(1)配制0.1 mol·L-1CuSO4溶液480 mL需要选择500mL容量瓶,其步骤为计算、称量、溶解、冷却、转移、洗涤、摇匀、定容、装瓶等操作,因此配制过程中需要的仪器为:托盘天平、药匙、烧杯、量筒、玻璃棒、胶头滴管、500 mL容量瓶等;
(2)实验室需配制480 mL 0.1 mol·L-1的CuSO4溶液,需要选用500 mL容量瓶,实际上配制的是500 mL 0.1 mol·L-1的硫酸铜溶液,需要硫酸铜的物质的量为0.1 mol·L-1×0.5 L=0.05 mol,若用CuSO4配制,则需要的质量为160 g·mol-1×0.05 mol=8.0 g;若用CuSO4·5H2O配制,则需要的质量为250 g·mol-1×0.05 mol=12.5 g,答案选AC;
(3)称量所用砝码生锈,称取的溶质的质量偏大,溶质的物质的量偏大,溶液的浓度偏高;
(4)溶解固体物质,用玻璃棒搅拌可以加速固体的溶解;
(5)配制一定物质的量浓度的溶液,在移液操作中应该用玻璃棒将溶液引流入容量瓶中,并洗涤烧杯2~3次,保证溶质全部转移到容量瓶中,防止产生误差;
(8)定容时,仰视刻度线,导致溶液的体积偏大,溶液的浓度偏低。


科目:高中化学 来源: 题型:
【题目】如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化过程中的颜色变化。实验时必须使用铁屑和6 mol·L1的硫酸,其他试剂任选。
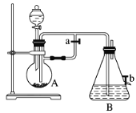
请回答下列问题:
(1)B中盛有一定量的NaOH溶液,A中应预先加入的物质是__________________,A中反应的离子方程式是____________________________________________________。
(2)实验开始时应先将活塞a________(填“打开”或“关闭”)。其目的是____________________。
(3)简述生成Fe(OH)2的操作过程:__________________________________________。
(4)实验完毕,打开b处活塞,放入一部分空气,此时B中发生反应的化学方程式为_________________。
(5)图中________(填“能”或“不能”)较长时间看到Fe(OH)2白色沉淀。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一个化学过程的示意图,回答下列问题:
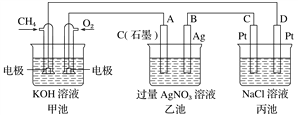
(1)甲池是_________装置,乙装置中电极A的名称是_____________。
(2)甲装置中通入O2的电极反应式为______________________,乙装置中电极B(Ag)的电极反应式为_____________________,丙装置中D极的产物是____________(写化学式)。
(3)一段时间,当丙池中产生气体共112 mL(标准状况)时,均匀搅拌丙池,所得溶液的pH=_____(温度为25 ℃时,并已知NaCl溶液足量,不考虑生成的气体在溶液中的溶解和反应,电解后溶液体积为500 mL)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验:
(1)若取a g样品,向其中加入足量的NaOH溶液,测得生成的气体(标准状况,下同)体积为b L。反应的化学方程式是___________________________________;样品中铝的质量为________g。
(2)另取a g样品将其点燃,恰好完全反应,该反应的化学方程式是2Al+Fe2O3![]() 2Fe+Al2O3,氧化铁与铝的质量比是________。
2Fe+Al2O3,氧化铁与铝的质量比是________。
(3)待(2)中反应产物冷却后,加入足量盐酸,测得生成的气体体积为c L,该气体与(1)中所得气体的体积比c∶b=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是中学化学中常见的三种物质,它们之间的相互转化关系如下图所示(部分反应条件及产物略去):
![]()
(1)若A是一种金属,C是淡黄色固体,则B的化学式为______,A→C反应的化学方程式为_________。
(2)若A是一种非金属,其常见单质为黑色固体,C是最主要的温室气体,则C的分子式为_______,B→C反应的化学方程式为___。
A和C是否可以发生反应______(填“能”或“不能”),若能,反应的化学方程式为____________(若不能,此空不填)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.工业上生产水泥和玻璃都要用石灰石做原料
B.玻璃钢是一种合金材料
C.除去氨气中的水蒸气可用无水氯化钙可做干燥剂
D.溶于水可以导电的化合物一定是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将二氧化碳转化为燃料是目前的研究热点,2017年《科学》杂志报道的一种将CO2转化为烃和醇的装置如图所示。下列说法正确的是

A. 图中能量转化的方式只有1种
B. 装置工作时,H+向X极区移动,Y极周围溶液的pH增大
C. X极上得到CH3OH的电极反应式为2CO2+4H2O+12e-==2CH3OH+3O2
D. 若X极生成1molC2H4和lmolCH3OH,电路中流过18mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有人曾建议用AG表示溶液的酸度,AG的定义为AG=lg![]() 。下列表述正确的是( )
。下列表述正确的是( )
A. 在25℃时,溶液的pH与AG的换算公式为AG=14+pH
B. 在25℃时,若溶液呈酸性,则pH<7,AG<0
C. 在25℃时,若溶液呈碱性,则pH>7,AG<0
D. 在25℃时,若溶液呈中性,则pH=7,AG=1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据反应原理设计的应用,不正确的是
A. CO32-+H2O![]() HCO3-+OH-:用热的纯碱溶液清洗油污
HCO3-+OH-:用热的纯碱溶液清洗油污
B. A13++3H2O![]() Al(OH)3(胶体)+3H+:明矾净水
Al(OH)3(胶体)+3H+:明矾净水
C. TiCl4+(x+2)H2O(过量)![]() TiO2·xH2O↓+4HCl:制备TiO2纳米粉
TiO2·xH2O↓+4HCl:制备TiO2纳米粉
D. SnCl2+H2O![]() Sn( OH)Cl↓+HCl配制氯化亚锡溶液时加入氢氧化钠溶液
Sn( OH)Cl↓+HCl配制氯化亚锡溶液时加入氢氧化钠溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com