
| A. | 钠着火后,可用泡沫灭火器来灭火 | |
| B. | 氧化钠和过氧化钠都属于碱性氧化物 | |
| C. | 过氧化钠与水的反应中,Na2O2作氧化剂,水作还原剂 | |
| D. | 用洁净的玻璃管向包有Na2O2的脱脂棉吹气,脱脂棉燃烧,说明CO2、H2O与Na2O2的反应是放热反应 |
分析 A.钠燃烧生成过氧化钠,过氧化钠能和水、二氧化碳反应生成氧气,钠和水反应生成可燃性气体氢气;
B.和酸反应只生成盐和水的氧化物是碱性氧化物;
C.过氧化钠与水的反应生成氢氧化钠与氧气,水中各元素的化合价不变,而Na2O2中-1价的氧变成0价和-2价;
D.过氧化钠和二氧化碳、水反应是氧化还原反应是放热反应.
解答 解:A.钠燃烧生成过氧化钠,过氧化钠能和水、二氧化碳反应生成氧气,钠和水反应生成可燃性气体氢气,氧气具有助燃性、氢气具有可燃性,所以Na燃烧不能用泡沫灭火器来灭火,应该用沙土灭火,故A错误;
B.和酸反应只生成盐和水的氧化物是碱性氧化物,过氧化钠和酸反应除了生成盐外还生成氧气,所以过氧化钠不是碱性氧化物,故B错误;
C.过氧化钠与水的反应生成氢氧化钠与氧气,水中各元素的化合价不变,而Na2O2中-1价的氧变成0价和-2价,所以水既不是氧化剂也不是还原剂,过氧化钠既是氧化剂以是还原剂,故C错误;
D.CO2、H2O与Na2O2反应是放热反应,放出的热量达到脱脂棉的着火点,所以脱脂棉着火,故D正确;
故选D.
点评 本题考查钠及其化合物的性质,为高频考点,侧重考查学生对基础知识的掌握,明确元素化合物性质及基本概念内涵是解本题关键,比较容易.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:解答题
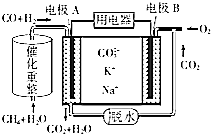 CH4和H2O(g)可发生催化重整反应:CH4(g)+H2O(g)?CO(g)+3H2(g).
CH4和H2O(g)可发生催化重整反应:CH4(g)+H2O(g)?CO(g)+3H2(g).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
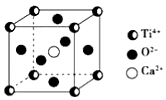 CaTiO3的晶体结构模型如图所示(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶角),下列关于晶体的说法正确的是( )
CaTiO3的晶体结构模型如图所示(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶角),下列关于晶体的说法正确的是( )| A. | CaTiO3的摩尔质量为136 | |
| B. | CaTiO3晶体中每个Ti4+与12个Ca2+紧相邻 | |
| C. | CaTiO3晶体中每个Ti4+与12个O2-紧相邻 | |
| D. | CaTiO3晶体中每个Ti4+与12个Ti4+紧相邻 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | HCO3-、ClO-、Na+、H+ | B. | Cl-、NH4+、NO3-、H+ | ||
| C. | K+、Cu2+、Cl-、SO42- | D. | OH-、Mg2+、Na+、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
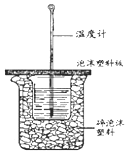 50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:
50ml0.50mol•L-1盐酸与50mL0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3溶液浸泡,再加入盐酸溶解 | |
| B. | 实验室制氢气,为了加快反应速率,可向稀H2SO4中滴加少量 Cu(NO3)2溶液 | |
| C. | N2(g)+3H2(g)?2NH3(g)△H<0,降低温度时:v(正)增大,v (逆)减小,平衡时氢气转化率增大 | |
| D. | 吸热反应“TiO2(s)+2Cl2(g)═TiCl4(g)+O2(g)”在一定条件下可自发进行,则该反 应的△S<0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com