
25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
A.澄清透明的溶液中:K+、Al3+、SO42-、MnO4-
B.1.0 mol•L-1FeCl3溶液中:Na+、Cl-、NO3-、SCN-
C.1.0 mol•L-1KNO3溶液中:Fe2+、H+、Cl-、SO42-
D.中性溶液中:Fe3+、Na+、Br?、SO42-
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年广西桂林市高三上学期期中考化学试卷(解析版) 题型:选择题
下列实验操作能达到预期实验目的的是 ( )
A.为检验卤代烃中的卤原子,先加入NaOH溶液加热,再滴入AgNO3溶液观察颜色变化
B.为检验醛基的存在,先向试管中加入2 mL 2%的NaOH溶液和数滴CuSO4溶液,再加乙醛,煮沸
C.为制取乙酸乙酯,将稀H2SO4和乙醇、乙酸混合加热,放出的蒸气通入盛有Na2CO3溶液的试管中
D.为制取乙烯,将稀H2SO4和乙醇混合加热
查看答案和解析>>
科目:高中化学 来源:2017届宁夏银川市高三上学期第三次月考化学试卷(解析版) 题型:填空题
【化学——选修3:物质结构】砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式 。
(2)根据元素周期律,原子半径Ga As,第一电离能Ga As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为 ,其中As的杂化轨道类型为 。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是 。
(5)GaAs的熔点为1238℃,密度为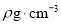 ,其晶胞结构如图所示。
,其晶胞结构如图所示。
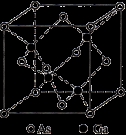
该晶体的类型为 。Ga与As的摩尔质量分别为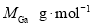 和
和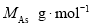 ,原子半径分别为
,原子半径分别为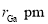 和
和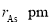 ,阿伏加德罗常数值为
,阿伏加德罗常数值为 ,则
,则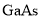 晶胞中原子的体积占晶胞体积的百分率为 。(已知1m=1012pm)
晶胞中原子的体积占晶胞体积的百分率为 。(已知1m=1012pm)
查看答案和解析>>
科目:高中化学 来源:2017届宁夏银川市高三上学期第三次月考化学试卷(解析版) 题型:选择题
下列有关实验装置进行的相应实验,不能达到实验目的的是
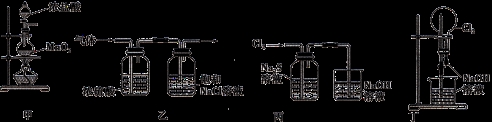
A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢和水蒸气
C.用装置丙可证明Cl2的氧化性强于S
D.用装置丁可以完成“喷泉”实验
查看答案和解析>>
科目:高中化学 来源:2017届吉林省吉林市高三毕业班第一次调研测化学试卷(解析版) 题型:选择题
在光的照射下,不能发生反应的是
A.O2与H2 B.F2与H2 C.Cl2与H2 D.Cl2与CH4
查看答案和解析>>
科目:高中化学 来源:2017届河南省豫北推荐高三上学期精英对抗赛化学试卷(解析版) 题型:填空题
氮氧化物是目前造成大气污染的主要气体。NO在空气中存在如下反应:

(1)上述反应分两步完成,其中第一步反应①如下,写出第二步反应②的热化学方程式(其反应的焓变
△H2用含△H、△H1的式子来表示):
①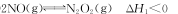
②________。
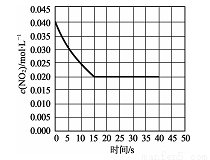
(2)在某温度下的一密闭容器中充人一定量的N02发生上述反应,测得NO2的浓度随时间的变化曲线如下图所示,前5秒内O2的平均生成速率为 mol.L-1.s-l,该条件下反应:2NO+O2 2NO2的化学平衡常数数值为 ,平衡后某时刻,升高反应体系的温度,建立新平衡状态后,测的混合气体的平均相对分子质量小于原平衡状态,则:2NO(g)+O2 (g)
2NO2的化学平衡常数数值为 ,平衡后某时刻,升高反应体系的温度,建立新平衡状态后,测的混合气体的平均相对分子质量小于原平衡状态,则:2NO(g)+O2 (g) 2NO2 (g)△H (填“>”或“<”)0。
2NO2 (g)△H (填“>”或“<”)0。
(3)2NO(g)+O2(g) 2NO2 (g)的两步反应中,反应①的反应速率数值较大,是一个快反应,会快速建立平衡状态,而反应②是一个慢反应,则决定反应2NO(g)+O2 (g)
2NO2 (g)的两步反应中,反应①的反应速率数值较大,是一个快反应,会快速建立平衡状态,而反应②是一个慢反应,则决定反应2NO(g)+O2 (g) 2NO2 (g)反应速率的是反应________(填“①”或“②”);对(2)中反应体系升高温度的过程中,发现2NO(g)+O2 (g)
2NO2 (g)反应速率的是反应________(填“①”或“②”);对(2)中反应体系升高温度的过程中,发现2NO(g)+O2 (g) 2NO2 (g)的反应速率变慢,结合该反应的两步反应过程分析可能的原因: (反应未使用催化剂)。
2NO2 (g)的反应速率变慢,结合该反应的两步反应过程分析可能的原因: (反应未使用催化剂)。
(4)若(2)中反应体系,反应开始时使用催化剂,请在(2)的图中画出该反应体系反应进程可能的曲线。
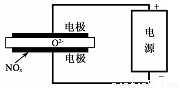
(5)电解法处理氮氧化物是目前大气污染治理的一个新思路。其原理是将NO.在电解池中分解成无污染的N2和02除去,如图所示,,两电极间是固体氧化物电解质,在一定条件下可自由传导O2-。则电解池阴极的电极反应式为_____________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省高一上月考三化学卷(解析版) 题型:选择题
常温下,在溶液中可以发生反应:X+2Y3+==2Y2++X2+,对下列叙述的判断正确的是( )
①X被氧化 ②X是氧化剂 ③X具有还原性 ④Y2+是氧化产物
⑤Y2+具有还原性 ⑥Y3+的氧化性比X2+的氧化性强
A.②③④⑥ B.①③④⑤ C.①③⑤⑥ D.①②⑤⑥
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上期中化学卷(解析版) 题型:选择题
氨氮废水中 的氮元素多以NH4+和NH3·H2O的形式存在,在一定条件下,NH4+经过两步反应被氧化成NO3?,两步反应的能量变化示意图如下:
的氮元素多以NH4+和NH3·H2O的形式存在,在一定条件下,NH4+经过两步反应被氧化成NO3?,两步反应的能量变化示意图如下:
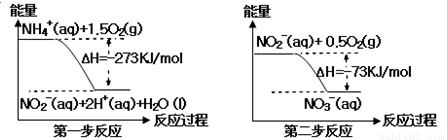
下列说法合理的是( )
A.该反应的催化剂是NO2?
B.升高温度,两步反应速率均加快,有利于NH4+ 转化成NO3?
C.在第一步反应中,当溶液中水的电离程度不变时,该反应即达平衡状态
D.1 mol NH4+在第一步反应中与1 mol NO2-在第二步反应中失电子数之比为1:3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com