

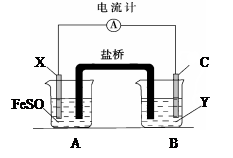
| A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法 |
| B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,溶液中的阳离子向铁电极移动 |
| C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动 |
| D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小 |
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案科目:高中化学 来源:不详 题型:单选题
| A.脱氧过程是吸热反应,可降低温度,延长食品保质期 |
| B.脱氧过程中铁作原电池正极,电极反应为:Fe-3e-=Fe3+ |
| C.脱氧过程中碳做原电池负极,电极反应为:2H2O+O2+4e-=4OH- |
| D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Li2S2O4。下列说法正确的是 ( )
Li2S2O4。下列说法正确的是 ( )| A.该电池反应为可逆反应 |
| B.放电时,Li+向负极移动 |
| C.充电时,阴极反应式为Li++e-=Li |
| D.该电池的电解质溶液可以换成LiBr的水溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Nio+M+H2O(M为储氢合金,电解质
Nio+M+H2O(M为储氢合金,电解质| A.充电过程中,电池的负极上发生的反应为H2O +M+ e- =MH+OH- |
| B.储氢合金位于电池的负极 |
| C.放电时,OH-离子向电池的负极移动 |
| D.充电过程中,化学能转化为电能储存在电池中 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀 |
| B.铅蓄电池放电时的负极和充电时的阳极均发生还原反应 |
| C.电解AlCl3、FeCl3、CuCl2的混合溶液时阴极上依次析出Cu、Fe、Al |
| D.电解食盐水一段时间后,可通入一定量的HCl气体来恢复原溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
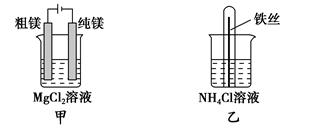
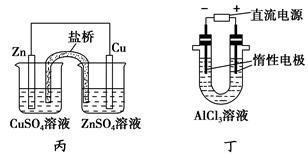
| A.用甲装置电解精炼镁 |
| B.用乙装置验证试管中铁丝发生析氢腐蚀 |
| C.用丙装置构成铜锌原电池 |
| D.用丁装置利用电冶金法制铝 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原电池工作时,阴离子移向正极 |
| B.铁片表面镀锌,铁片接电源负极 |
| C.用Cu作电极电解H2O,阳极反应为:4OH--4e-===2H2O+O2↑ |
| D.向AgCl饱和溶液中加入NaCl固体,c (Cl-)增大,Ksp增大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
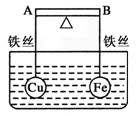
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com