
| A. |  配制一定物质的量浓度的稀硫酸 | B. | 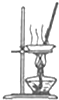 蒸发NH4Cl饱和溶液制备NH4Cl晶体 | ||
| C. | 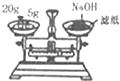 称量NaOH固体 | D. | 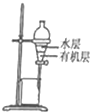 萃取后有机层从下口排放 |
分析 A.不能在容量瓶中稀释浓硫酸;
B.氯化铵易分解;
C.氢氧化钠应放在左盘,且放在小烧杯中;
D.有机层在下层,从下端分离.
解答 解:A.浓硫酸溶于水放出大量的热,而容量瓶只能在常温下使用,不能在容量瓶中稀释浓硫酸,故A错误;
B.氯化铵易分解生成氨气和氯化氢,所以得不到氯化铵晶体,不能用直接加热的方法分离,故B错误;
C.氢氧化钠应放在左盘,因氢氧化钠易潮解,应放在小烧杯中,故C错误;
D.有机层在下层,从下端分离,故D正确.
故选D.
点评 本题考查化学实验方案评价,为高频考点,涉及物质制备、分离、仪器的使用等知识点,明确实验原理、物质性质差异性、仪器的用途等是解本题关键,侧重考查学生观察分析判断能力,难度中等.


 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 最外层电子数为1的原子都为金属元素的原子 | |
| B. | 最外层电子数为8的微粒是稀有气体元素的原子 | |
| C. | 在元素周期表里,元素所在的周期数等于原子核外电子层数 | |
| D. | 在元素周期表里,主族元素所在的族的序数等于原子核外电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 测定其导电性能相同 | |
| B. | 与足量的锌粉反应的起始速率相同 | |
| C. | 与足量的锌粉反应产生氢气的体积比为1:1:100 | |
| D. | 与同浓度氢氧化钠溶液反应,消耗氢氧化钠溶液的体积为1:2:100 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘化钾与氯气:5I-+3Cl2-+3H2O→IO3-+6Cl-+6H+ | |
| B. | KAl(SO4)2与Ba(OH)2:2Ba2++4OH-+Al3++2SO42-→2BaSO4↓+AlO2-+2H2O | |
| C. | 氨水与SO2:NH3•H2O+SO2→HSO3-+NH4+ | |
| D. | NaAlO2与AlCl3:Al3++3AlO2-+6H2O→4Al (OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 37g该氯气样品含NA个氯气分子 | |
| B. | 11.2L该氯气样品质量是37g | |
| C. | 37g该氯气样品与足量NaOH完全反应生成Na37Cl和Na37ClO3,氧化剂和还原剂的质量之比为5:1 | |
| D. | 0.1NA个氯气分子溶于水形成1000mL溶液,溶液中c(Cl-)=0.2mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
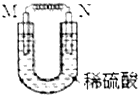 如图所示装置中,M为活动性顺序位于氢之前的金属,N为石墨棒.关于此装置的下列叙述中,不正确的是( )
如图所示装置中,M为活动性顺序位于氢之前的金属,N为石墨棒.关于此装置的下列叙述中,不正确的是( )| A. | N上有气体放出 | |
| B. | M为负极,N为正极 | |
| C. | 导线中有电流通过,电流方向是由M到N | |
| D. | 该装置是化学能转变为电能的装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
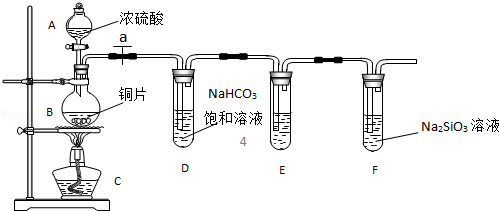
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com