
| A. | 碘-131原子核外有5个电子层 | |
| B. | 碘-131原子的最外层有7个电子 | |
| C. | 具有放射性的碘-131原子比普通碘-127原子多4个中子 | |
| D. | 131I2与127I2互为同位素 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:填空题
 NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控.
NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加压强 | B. | 加大水量 | C. | 升高温度 | D. | 加入催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 如图所示 表示乙醇的比例模型 表示乙醇的比例模型 | |
| B. | 蔗糖、纤维素的水解过程都是高分子转化为小分子的过程 | |
| C. | 甲烷、甲醛、甲酸都不存在同分异构体,则甲醚(CH3OCH3)也不存在同分异构体 | |
| D. | HOCH2COOH既可以发生取代反应又可以发生缩聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 反应时间/min | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 烧杯和药品的总质量/g | 210.0 | 206.8 | 205.9 | 205.7 | 205.6 | 205.6 | 205.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | B | ||||||
| D | E | F | |||||
| C | I | G | H |
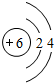 .
.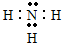 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温条件下,在空气中铝不容易被腐蚀 | |
| B. | 镀锌铁片比镀锡铁片更耐腐蚀 | |
| C. | 镀银的铁制品,镀层部分受损后,露出的铁表面易被腐蚀 | |
| D. | 远洋海轮的尾部装上一定数量的锌板 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O:0.002 mol•L-1 | B. | NO:0.001 mol•L-1 | ||
| C. | NH3:0.002 mol•L-1 | D. | O2:0.0025 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钠和稀盐酸反应:CO32-+2H+=H2O+CO2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-=Al(OH)3↓ | |
| C. | 三氯化铁溶液中加入铁粉:Fe3++Fe=2Fe2+ | |
| D. | FeCl2溶液跟氯气反应:2Fe2++Cl2=2 Fe3++2Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com