B
分析:A.含有0.1molBaC1
2的溶液中C1
-的物质的量为0.2mol,根据N=nN
A计算氯离子数目;
B.根据n=

计算22gCO
2的物质的量,再根据N=nN
A计算二氧化碳分子数目;
C.二氧化碳所处的状态不一定是标准状况;
D.常温常压下,气体摩尔体积不是22.4L/mol,由pV=nRT可知,气体摩尔体积大于22.4L/mol.
解答:A.含有0.1molBaC1
2的溶液中C1
-的物质的量为0.2mol,故氯离子数目为0.2mol×N
Amol
-1=0.2N
A,故A错误;
B.22gCO
2的物质的量为
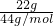
=0.5mol,故含有二氧化碳分子数目为0.5mol×N
Amol
-1=0.5N
A,故B正确;
C.二氧化碳所处的状态不一定是标准状况,11.2LCO
2的物质的量不一定是0.5mol,故C错误;
D.常温常压下,气体摩尔体积不是22.4L/mol,由pV=nRT可知,气体摩尔体积大于22.4L/mol,故N
A个C1
2分子所占有的体积大于22.4L,故D错误;
故选B.
点评:本题考查常用化学计量的有关计算,难度不大,注意气体摩尔体积的使用条件与对象.

 计算22gCO2的物质的量,再根据N=nNA计算二氧化碳分子数目;
计算22gCO2的物质的量,再根据N=nNA计算二氧化碳分子数目;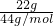 =0.5mol,故含有二氧化碳分子数目为0.5mol×NAmol-1=0.5NA,故B正确;
=0.5mol,故含有二氧化碳分子数目为0.5mol×NAmol-1=0.5NA,故B正确;

 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案