
·ÖĪö £Ø1£©ŌŚ»¹ŌŃõ»ÆĢśµÄ·“Ó¦ÖŠĢ¼¼ČæÉŅŌ±»Ńõ»ÆÉś³ÉCO£¬Ņ²æÉÄܱ»Ńõ»ÆÉś³ÉCO2£¬¹Ź¼ŁÉč¢ŪÓ¦ŹĒCO2”¢COµÄ»ģŗĻĪļ£»
£Ø2£©·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬ļ§øłĄė×ÓÓėŃĒĻõĖįĄė×ÓÉś³ÉµŖĘų”¢Ė®£»
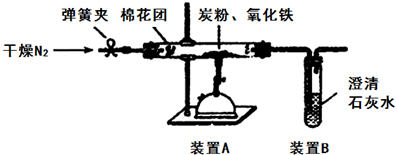
£Ø3£©·ĄÖ¹æÕĘų²ĪÓė·“Ó¦£¬ŹµŃéĒ°ÓƵŖĘųÅž”×°ÖĆÖŠµÄæÕĘų£®ŹµŃé½įŹųŗó£¬Č·±£·“Ó¦µĆµ½µÄCO2Č«²æĶعżB×°ÖĆ£»
£Ø4£©øł¾Ż¢ŻæÉÖŖÉś³ÉĪļCO2µÄĪļÖŹµÄĮæŹĒ$\frac{2.00g}{100g/mol}$=0.02mol£¬ĘäÖŹĮæŹĒ0.88g£¬øł¾Ż¢ÜæÉÖŖ·“Ó¦ÖŠÉś³ÉµÄĘųĢå¹²48.48g+3.2g+2.0g-52.24g=1.44g£¬Ņņ“ĖCOµÄÖŹĮæŹĒ1.44g-0.88g=0.56g£¬ĘäĪļÖŹµÄĮæŹĒ$\frac{0.56g}{28g/mol}$=0.02mol£¬¼“COŗĶCO2µÄĢå»żÖ®±ČŹĒ1£ŗ1£»
£Ø5£©¢ŁĒāŃõ»ÆøʵÄČܽā¶ČŠ”£¬ĪüŹÕCO2µÄŠ§¹ū²ī£¬ĒāŃõ»Æ±µµÄČܽā¶Č“ó£¬ĪüŹÕCO2µÄŠ§¹ūŅŖŗĆ£¬ĒŅĢ¼Ėį±µµÄĻą¶Ō·Ö×ÓÖŹĮæ“óÓŚĢ¼ĖįøĘµÄ£¬³ĘĮæŹ±Īó²īŠ”£»
¢ŚCOÓŠ¶¾£¬Ņņ“ĖŅŖÓŠĪ²Ęų“¦Ąķ×°ÖĆ£®
½ā“š ½ā£ŗ£Ø1£©ŌŚ»¹ŌŃõ»ÆĢśµÄ·“Ó¦ÖŠĢ¼¼ČæÉŅŌ±»Ńõ»ÆÉś³ÉCO£¬Ņ²æÉÄܱ»Ńõ»ÆÉś³ÉCO2£¬¹Ź¼ŁÉč¢ŪÓ¦ŹĒCO2”¢COµÄ»ģŗĻĪļ£¬¹Ź“š°øĪŖ£ŗCO2”¢COµÄ»ģŗĻĪļ£»
£Ø2£©·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬ļ§øłĄė×ÓÓėŃĒĻõĖįĄė×ÓÉś³ÉµŖĘų”¢Ė®£¬·“Ó¦Ąė×Ó·½³ĢŹ½ĪŖNH4++NO2-$\frac{\underline{\;\;”÷\;\;}}{\;}$N2”ü+2H2O£¬¹Ź“š°øĪŖ£ŗNH4++NO2-$\frac{\underline{\;\;”÷\;\;}}{\;}$N2”ü+2H2O£»
£Ø3£©ŹµŃé¹ż³ĢÖŠÓ¦·ĄÖ¹æÕĘų²ĪÓė·“Ó¦£¬ĖłŅŌŹµŃéĒ°ÓƵŖĘųÅž”×°ÖĆÖŠµÄæÕĘų£®ŹµŃé½įŹųŗó£¬ĪŖĮĖ°ŃÉś³ÉµÄĘųĢåČ«²æÅųö£¬ÓÖŠčŅŖÓƵŖĘųÅž”Éś³ÉµÄĘųĢå£¬Č·±£·“Ó¦µĆµ½µÄCO2Č«²æĶعżB×°ÖĆ£¬
¹Ź“š°øĪŖ£ŗ·“Ó¦Ē°Åž”×°ÖĆÄŚµÄæÕĘų”¢Č·±£·“Ó¦µĆµ½µÄCO2Č«²æĶعżB×°ÖĆ£»
£Ø4£©øł¾Ż¢ŻæÉÖŖÉś³ÉĪļCO2µÄĪļÖŹµÄĮæŹĒ$\frac{2.00g}{100g/mol}$=0.02mol£¬ĘäÖŹĮæŹĒ0.88g£¬øł¾Ż¢ÜæÉÖŖ·“Ó¦ÖŠÉś³ÉµÄĘųĢå¹²48.48g+3.2g+2.0g-52.24g=1.44g£¬Ņņ“ĖCOµÄÖŹĮæŹĒ1.44g-0.88g=0.56g£¬ĘäĪļÖŹµÄĮæŹĒ$\frac{0.56g}{28g/mol}$=0.02mol£¬¼“COŗĶCO2µÄĢå»żÖ®±ČŹĒ1£ŗ1£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗFe2O3+2C$\frac{\underline{\;øßĪĀ\;}}{\;}$2Fe+CO”ü+CO2”ü£¬
¹Ź“š°øĪŖ£ŗFe2O3+2C$\frac{\underline{\;øßĪĀ\;}}{\;}$2Fe+CO”ü+CO2”ü£»
£Ø5£©¢ŁĒāŃõ»ÆøʵÄČܽā¶ČŠ”£¬ĪüŹÕCO2µÄŠ§¹ū²ī£¬ĒāŃõ»Æ±µµÄČܽā¶Č“ó£¬ĪüŹÕCO2µÄŠ§¹ūŅŖŗĆ£¬ĒŅĢ¼Ėį±µµÄĻą¶Ō·Ö×ÓÖŹĮæ“óÓŚĢ¼ĖįøĘµÄ£¬³ĘĮæŹ±Īó²īŠ”£¬
¹Ź“š°øĪŖ£ŗBa£ØOH£©2µÄČܽā¶Č“óÓŚCa£ØOH£©2£¬±£Ö¤²śÉśµÄCO2Č«²æ±»×°ÖĆBĪüŹÕ£¬±ÜĆāĘäŅŻ³öŌģ³É²ā¶ØĪó²ī£»
¢ŚCOÓŠ¶¾£¬Ņņ“ĖŅŖÓŠĪ²Ęų“¦Ąķ×°ÖĆ£¬¹Ź“š°øĪŖ£ŗƻӊĪ²Ęų“¦Ąķ×°ÖĆ£®
µćĘĄ ±¾ĢāÖ÷ŅŖŹĒæ¼²éŹµŃé·½°øÉč¼Ę”¢Ģ½¾æÓėĘĄ¼ŪµČ£¬×¢ŅāĢ½¾æŹµŃéµÄŅ»°ć²½Öč£¬Ė®¶Ōѧɜ×ŪŗĻÄÜĮ¦µÄ漲飬ĪŖøßæ¼³£æ¼ĢāŠĶ£¬×¢ŅāÕĘĪÕŌŖĖŲ»ÆŗĻĪļÖŖŹ¶£¬×¢ŅāŹµŃéÖŠÉųĶø»·±£ŅāŹ¶”¢¶ØĮæŹµŃéÖŠ×¼Č·ŠŌ£¬ÄѶČÖŠµČ£®


 ѧ¶ųÓÅŹīĘŚĻĪ½ÓÄĻ¾©“óѧ³ö°ęÉēĻµĮŠ“š°ø
ѧ¶ųÓÅŹīĘŚĻĪ½ÓÄĻ¾©“óѧ³ö°ęÉēĻµĮŠ“š°ø Happy holiday»¶ĄÖ¼ŁĘŚŹī¼Ł×÷Ņµ¹ć¶«ČĖĆń³ö°ęÉēĻµĮŠ“š°ø
Happy holiday»¶ĄÖ¼ŁĘŚŹī¼Ł×÷Ņµ¹ć¶«ČĖĆń³ö°ęÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
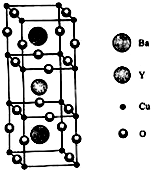 Ķ×åŌŖĖŲ°üĄØCu”¢Ag”¢Au£¬Ę䵄֏¾łĪŖĆęŠÄĮ¢·½¾§Ģ壮
Ķ×åŌŖĖŲ°üĄØCu”¢Ag”¢Au£¬Ę䵄֏¾łĪŖĆęŠÄĮ¢·½¾§Ģ壮²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŅŃÖŖ£ŗH2£Øg£©+$\frac{1}{2}$O2£Øg£©ØTH2O£Øl£©£»”÷H=-285.8 kJ•mol-1£¬ŌņH2µÄČ¼ÉÕČČĪŖ-285.8 kJ•mol-1 | |
| B£® | ŅŃÖŖ£ŗS£Øg£©+O2£Øg£©ØTSO2£Øg£©”÷H1=-Q1£»S£Øs£©+O2£Øg£©ØTSO2£Øg£©”÷H2=-Q2£¬ŌņQ1£¼Q2 | |
| C£® | ŅŃÖŖ£ŗ$\frac{1}{2}$H2SO4£ØÅØ£©+NaOH£Øaq£©ØT$\frac{1}{2}$Na2SO4£Øaq£©+H2O£Øl£©”÷H1£» CH3COOH£Øaq£©+NH3•H2O£Øaq£©ØTCH3COONH4£Øaq£©+H2O£Øl£©”÷H2£¬ŌņÓŠ|”÷H1|£¼|”÷H2| | |
| D£® | ŅŃÖŖ£ŗFe2O3£Øs£©+3C£ØŹÆÄ«£©ØT2Fe£Øs£©+3CO£Øg£©”÷H=+489.0 kJ•mol-1 CO£Øg£©+$\frac{1}{2}$O2£Øg£©ØTCO2£Øg£©”÷H=-283.0 kJ•mol-1 C£ØŹÆÄ«£©+O2£Øg£©ØTCO2£Øg£©”÷H=-393.5 kJ•mol-1 Ōņ4Fe£Øs£©+3O2£Øg£©ØT2Fe2O3£Øs£©”÷H=-1641.0 kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Ń”ÓĆŹŌ¼Į | ŹµŃéĻÖĻó | |
| ·½°ø1 | ||
| ·½°ø2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2FeO4 ÄÜÓėĖ®»ŗĀż·“Ӧɜ³ÉFe£ØOH£©3 ŗĶO2£¬¹ŹæÉÓĆ×÷Ė®µÄĻū¶¾¼ĮŗĶ¾»»Æ¼Į | |
| B£® | øÖĢś±ķĆęæ¾Ą¶Éś³ÉŅ»²ćÖĀĆܵÄFe3O4£¬ÄÜĘšµ½·ĄøÆŹ“×÷ÓĆ | |
| C£® | Ģ«ŃōÄÜ”¢·ēÄÜŹĒæÉŌŁÉśÄÜŌ“£¬Ó¦“óĮ¦ĶĘ¹ćĢ«ŃōÄÜ”¢·ēÄܵď¹ÓĆ | |
| D£® | ŠĀŠĶÄÜŌ“ÉśĪļ²ńÓĶŗĶæóĪļÓĶµÄÖ÷ŅŖ»Æѧ³É·ÖĻąĶ¬ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com