
���� ��1��������ʯ���鷴Ӧ�Ʊ�Ư�ۣ�
��2��Ư��Һ�Լ��ԣ�����Ư���ԣ�
��3������ͨ��ʯ����[Ca��OH��2]�з�Ӧ�����Ȼ��ơ�������ơ�ˮ��
��4��������SO2ͨ��Ư����Һ�У�����������ԭ��Ӧ��
��5��2NaClO3+4HCl�T2ClO2��+Cl2��+2NaCl+2H2O�У�2molHCl����ԭ����ת��2mol���ӣ�
��� �⣺��1��������ʯ���鷴Ӧ�Ʊ�Ư�ۣ���Ư�۵���Ч�ɷ���Ca��ClO��2���ʴ�Ϊ��Ca��ClO��2��
��2��������Һ�ȱ���ɫ����ɫ����֪Ư��Һ�Լ��ԣ�����Ư���ԣ��ʴ�Ϊ��BC��
��3������ͨ��ʯ����[Ca��OH��2]�з�Ӧ�����Ȼ��ơ�������ơ�ˮ����ӦΪ2Cl2+2Ca��OH��2�TCaCl2+Ca��ClO��2+2H2O��
�ʴ�Ϊ��2Cl2+2Ca��OH��2�TCaCl2+Ca��ClO��2+2H2O��
��4��������SO2ͨ��Ư����Һ�У�����������ԭ��Ӧ����Ca��ClO��2+SO2+H2O�TCaSO3��+2HClO����ȷ��
�ʴ�Ϊ������ȷ����Ϊ������ƣ�CaSO3������ǿ�Ļ�ԭ�ԣ��ᱻHClO������������ƣ�
��5��2NaClO3+4HCl�T2ClO2��+Cl2��+2NaCl+2H2O�У�2molHCl����ԭ����ת��2mol���ӣ���ת��0.2mol����ʱ���μӷ�Ӧ�Ļ�ԭ�������ʵ���Ϊ0.2mol��
�ʴ�Ϊ��0.2mol��
���� ���⿼�����ʵ����ʼ�Ӧ�ã�Ϊ��Ƶ���㣬�������ʵ����ʡ�������������ԭ��ӦΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
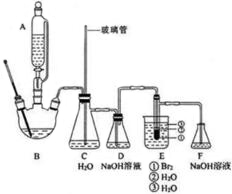 1��2-���������dz��õ��л��ϳ��м��壬ijС��������װ�úϳ�1��2-�������飮
1��2-���������dz��õ��л��ϳ��м��壬ijС��������װ�úϳ�1��2-�������飮| �е�/�� | �ܶ�/��g•cm-3�� | ˮ���ܽ��� | |
| 1��2-�������� | 131.4 | 2.18 | �� |
| �� | 58.8 | 3.12 | �� |
| �Ҵ� | 78.5 | 0.79 | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2��3-�������� | B�� | 3��3-�������� | ||
| C�� | 2-��-3-�һ����� | D�� | 2��2��3��3-�ļ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{W}{W+18a}$��100% | B�� | $\frac{W}{W+36a}$��100% | C�� | $\frac{W}{161��W+18a��}$��100% | D�� | $\frac{W}{161��W+36a��}$��100% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������Ӽ����������Ǽ��Լ� | B�� | ��������Լ����Ǽ��Լ� | ||
| C�� | ��������Լ������Ӽ������� | D�� | ���Ӽ���������������Ǽ��Լ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
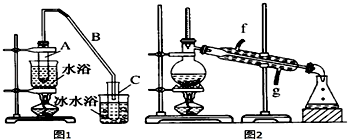

| �ܶȣ�g/cm3�� | �۵㣨�棩 | �е㣨�棩 | �ܽ��� | |
| ������ | 0.96 | 25 | 161 | ������ˮ |
| ����ϩ | 0.81 | -103 | 83 | ������ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�Ӧ�е�Ԫ�ر����� | |
| B�� | �÷�Ӧ��H2O2����ԭ�� | |
| C�� | ʵ��������NaCN��Һʱ�������������NaOH��Һ | |
| D�� | �����£�Ũ�Ⱦ�Ϊ0.1 mol•L-1 NaCN��NaHCO3��Һ��ǰ�ߵ�pHС�ں��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
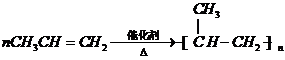 ��
�� ��
��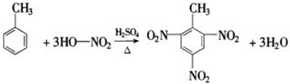 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com