
 .
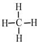
.| 12n |
| 12n+2n+2 |
 ,故答案为:
,故答案为: .
.


科目:高中化学 来源: 题型:
 如图甲为用氢气还原氧化铜的微型快速实验装置,实验前先将铜丝1处理成下端弯曲的一小圆环,并用铁锤锤击成带小孔的小匙,将铜丝2一段弯曲成螺旋状,试回答下列问题:
如图甲为用氢气还原氧化铜的微型快速实验装置,实验前先将铜丝1处理成下端弯曲的一小圆环,并用铁锤锤击成带小孔的小匙,将铜丝2一段弯曲成螺旋状,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v正(N2)=v 逆(NH3) |
| B、3v正(N2)=v 正(H2) |
| C、2v正(H2)=3v 逆(NH3) |
| D、v正(N2)=3v 逆(H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、第3周期所含元素中钠的第一电离能最小 |
| B、在所有元素中,氟的第一电离能最大,铝的第一电离能比镁的第一电离能大 |
| C、元素的第一电离能:Cl比Na小 |
| D、钾的第一电离能比镁的第一电离能大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某化学兴趣小组的同学通过以下实验确定炭粉与Na2O2反应的产物.
某化学兴趣小组的同学通过以下实验确定炭粉与Na2O2反应的产物.
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 ①如图中,锥形瓶内盛有气体X,滴管内盛有液体Y.若挤压滴管胶头,使液体Y滴入瓶中,振荡,过一会可见小气球a鼓气.气体X和液体Y可能是(完成下列表格)
①如图中,锥形瓶内盛有气体X,滴管内盛有液体Y.若挤压滴管胶头,使液体Y滴入瓶中,振荡,过一会可见小气球a鼓气.气体X和液体Y可能是(完成下列表格)| 气体X | Cl2 | ||
| 液体Y | H2O | NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验目的 | 实验方法 | |
| A | 分离水和酒精 | 分液 |
| B | 从食盐水中获得食盐 | 过滤 |
| C | 将海水淡化为可饮用水 | 蒸馏 |
| D | 除去碳酸氢钠固体中的碳酸钠 | 加热 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com