
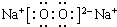 .
. 分析 ①H2O中只含O-H共价键;
②H2O2中含O-H极性共价键和O-O非极性共价键;
③Ba(OH)2中含O-H极性共价键和离子键;
④Na2O2中含O-O非极性共价键和离子键;
⑤Cl2中含Cl-Cl非极性共价键;
⑥Ar中不含化学键;
⑦CO2中只含C、O之间极性共价键.
解答 解:①H2O中只含O-H共价键;
②H2O2中含O-H极性共价键和O-O非极性共价键;
③Ba(OH)2中含O-H极性共价键和离子键;
④Na2O2中含O-O非极性共价键和离子键;
⑤Cl2中含Cl-Cl非极性共价键;
⑥Ar中不含化学键;
⑦CO2中只含C、O之间极性共价键,
(1)由离子键和非极性键构成的是④,故答案为:④;
(2)由极性键和非极性键构成的是②,故答案为:②;
(3)不存在化学键的是⑥,故答案为:⑥;
(4)共价化合物有①②⑦,故答案为:①②⑦;
(5)Na2O2的电子式为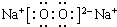 ,故答案为:
,故答案为: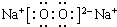 .
.
点评 本题考查化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 燃烧、酸碱中和反应都是放热反应 | |
| B. | 化学反应必然伴随着能量的变化 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 反应物总能量和生成物总能量的相对大小决定了反应是放出能量还是吸收能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
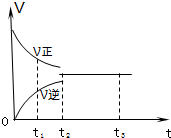 如图是可逆反应3X2+Y2?2Z2 在反应过程中的反应速率(V)与时间(t)的关系曲线,下列叙述正确的是( )
如图是可逆反应3X2+Y2?2Z2 在反应过程中的反应速率(V)与时间(t)的关系曲线,下列叙述正确的是( )| A. | t1时,只有正方向反应没有逆方向反应 | |
| B. | t2时,反应已达到平衡状态 | |
| C. | t2-t3,各物质的浓度不再发生变化 | |
| D. | t2-t3,处于静止状态,反应不再发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:HClO4>H2SO4>H3PO4 | B. | 碱性:KOH>NaOH>LiOH | ||
| C. | 单质的氧化性:F2<Cl2<Br2<I2 | D. | 单质的还原性:Al<Mg<Na |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2通入品红溶液 | B. | 碘酒滴入淀粉溶液 | ||
| C. | 乙烯通入酸性KMnO4溶液中 | D. | Cl2通入NaOH溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的密度不再改变 | |
| B. | 混合气体的平均分子量不再改变 | |
| C. | 混合气体中,N2、H2、NH3的物质的量之比为1:3:2 | |
| D. | 1个N≡N键断裂的同时,有6个N-H键形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 的键线式
的键线式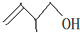
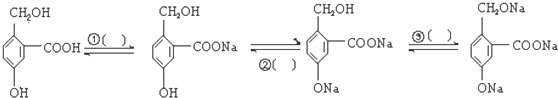
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com