
���û�ѧ��Ӧԭ���о��������ȡ���ȵ��ʼ��仯����ķ�Ӧ����Ҫ���塣
���������У�SO2����������SO3��2SO2(g)��O2(g)  2SO3(g)�������ϵ��SO3�İٷֺ������¶ȵĹ�ϵ����ͼ��ʾ(�������κ�һ�㶼��ʾƽ��״̬)������ͼʾ�ش��������⣺
2SO3(g)�������ϵ��SO3�İٷֺ������¶ȵĹ�ϵ����ͼ��ʾ(�������κ�һ�㶼��ʾƽ��״̬)������ͼʾ�ش��������⣺
(1)2SO2(g)��O2(g)  2SO3(g)�Ħ�H________0(�>����<��)�����ں��£���ѹ������������ƽ����ϵ��ͨ�뺤����ƽ��________�ƶ�(��������ҡ�����)��
2SO3(g)�Ħ�H________0(�>����<��)�����ں��£���ѹ������������ƽ����ϵ��ͨ�뺤����ƽ��________�ƶ�(��������ҡ�����)��
(2)���¶�ΪT1��T2����Ӧ��ƽ�ⳣ���ֱ�ΪK1��K2����K1________K2������Ӧ���е�״̬Dʱ��v��________v��(�>����<������)��
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
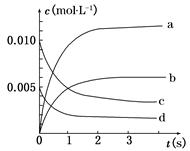
��2 L�ܱ������ڣ�800��ʱ��Ӧ2NO(g)��O2(g)  2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
| ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ij�¶�ʱ,��2 L������,ijһ��Ӧ��A��B�����ʵ�����ʱ��仯����������ͼ��ʾ,��ͼ�����ݷ�����: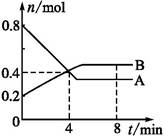
(1)��4 minĩʱ,A��B�����ʵ���Ũ��c(A)��������c(B),��0~4 min��A��B�����ʵ���Ũ�ȱ仯����c(A)����������c(B)(�����>����<����=��)��
(2)�ӷ�Ӧ��ʼ��4 minʱ,A��ƽ����Ӧ����Ϊ������
(3)�÷�Ӧ�Ļ�ѧ����ʽΪ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�������ʵ�����A��B��C��D�������ʻ�Ϸ���V L�ܱ�������,�������·�Ӧ:aA+bB cC(s)+dD,����Ӧ���е���t minʱ,���A������n mol,B������n/2 mol,C������3n/2 mol,D������n mol����ʱ��Ӧ�ﵽƽ�⡣
cC(s)+dD,����Ӧ���е���t minʱ,���A������n mol,B������n/2 mol,C������3n/2 mol,D������n mol����ʱ��Ӧ�ﵽƽ�⡣
(1)�û�ѧ����ʽ��,�����ʵĻ�ѧ�������ֱ�Ϊ:a=��������,b=��������,c=��������,d=����������
(2)��B��Ũ�ȱ仯��ʾ�ĸû�ѧ��Ӧ������Ϊv(B)=����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�ϳɰ����������Ĵ����������˹��̵���;�����Ի�ѧ��ҵ����Ҳ�������ش�Ӱ�졣�ϳɰ���Ӧ�Ļ�ѧ����ʽΪN2(g)��3H2(g) 2NH3(g)����H����92.2 kJ��mol��1���ϳɰ���ҵ��ԭ����N2�ɴӿ����з���õ���H2���ü����̿��ˮ������Ӧ�Ƶá�
2NH3(g)����H����92.2 kJ��mol��1���ϳɰ���ҵ��ԭ����N2�ɴӿ����з���õ���H2���ü����̿��ˮ������Ӧ�Ƶá�
(1)��һ�ݻ��̶����ܱ�������ע��N2��H2�������壬����������Ӧ����ij�¶��´ﵽƽ��ʱ�������ʵ�Ũ�ȷֱ��ǣ�c(H2)��9.00 mol��L��1��c(N2)��3.00 mol��L��1��c(NH3)��4.00 mol��L��1�����¶��¸÷�Ӧ��ƽ�ⳣ��K��________��
(2)��������ͬ�����и�����1 mol N2��3 mol H2���ڲ�ͬ�����·�Ӧ���ﵽƽ�⣬�������������ʱ��仯��������ͼ��ʾ������˵������ȷ����________(����ĸ)��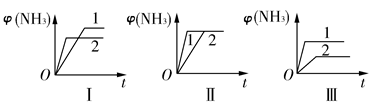
| A��ͼ������Dz�ͬѹǿ�Է�Ӧ��Ӱ�죬��p2>p1 |
| B��ͼ������Dz�ͬѹǿ�Է�Ӧ��Ӱ�죬��p1>p2 |
| C��ͼ������Dz�ͬ�¶ȶԷ�Ӧ��Ӱ�죬��T1>T2 |
| D��ͼ�������ͬ��ͬѹ�²�ͬ�����Է�Ӧ��Ӱ�죬�Ҵ�������1>2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ij̽����ѧϰС������ͬ������п����ͬŨ�ȵ�������ϡ���ᷴӦ�õ�ʵ���������±���ʾ��
| ʵ���� | п��״̬ | ��Ӧ�¶�/�� | �ռ�100 mL���� ����ʱ��/s |
| �� | ��Ƭ | 15 | 200 |
| �� | ��Ƭ | 25 | 90 |
| �� | ��ĩ | 25 | 10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ѧѧ���еĻ�ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ���������������ԭ����
��ش��������⣺ ��1����ҵ�ϲ�ȡCO��H2Ϊԭ�Ϻϳ��Ҵ����仯ѧ��Ӧ����ʽΪ��2CO��g����4H2��g��??
��1����ҵ�ϲ�ȡCO��H2Ϊԭ�Ϻϳ��Ҵ����仯ѧ��Ӧ����ʽΪ��2CO��g����4H2��g��??
CH3CH2OH��g����H2O��g������д���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK��________��
��2�������£�Ũ�Ⱦ�Ϊ0.1 mol��L��1��������Һ��pH���±���
| ���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | Na2SO4 |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 7.0 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��1��N2��g����3H2��g��  2NH3��g������H����94.4 kJ��mol��1������ʱ����ϵ�и�����Ũ����ʱ��仯��������ͼ��ʾ��
2NH3��g������H����94.4 kJ��mol��1������ʱ����ϵ�и�����Ũ����ʱ��仯��������ͼ��ʾ��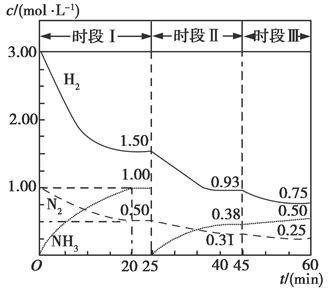
����1 L�����з�����Ӧ��ǰ20 min�ڣ�v��NH3����________���ų�������Ϊ________��
��25 minʱ��ȡ�Ĵ�ʩ��_______________________��
��ʱ�������·�Ӧ��ƽ�ⳣ������ʽΪ________���þ������ݱ�ʾ����
��2���糧�������뵪������Ӧ�٣�4NH3��g����6NO��g�� 5N2��g����6H2O��g��������Ӧ�ڣ�2NH3��g����8NO ��g��
5N2��g����6H2O��g��������Ӧ�ڣ�2NH3��g����8NO ��g��  5N2O��g����3H2O��g������H��0�����ƽ��������N2��N2O�������¶ȵĹ�ϵ��ͼ����400��600 Kʱ��ƽ��������N2�������¶ȵı仯������________���������ֱ仯���ɵ�ԭ����________���δ������һ��ԭ��
5N2O��g����3H2O��g������H��0�����ƽ��������N2��N2O�������¶ȵĹ�ϵ��ͼ����400��600 Kʱ��ƽ��������N2�������¶ȵı仯������________���������ֱ仯���ɵ�ԭ����________���δ������һ��ԭ��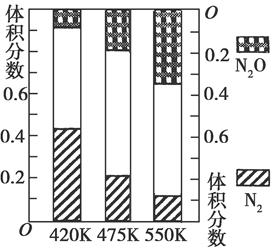
��3��ֱ�ӹ���ʽȼ�ϵ������NaOH��ҺΪ����ʵġ���ط�ӦΪ4NH3��3O2=2N2��6H2O�����缫��ӦʽΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�ݱ���,��300 �桢70 MPa ������,��CO2��H2�ϳ��Ҵ��ѳ�Ϊ��ʵ,�úϳɶԽ����Դ��������ش����塣
(1)��֪25 �桢101 kPa������,1 g�Ҵ�ȼ������CO2��Һ̬ˮʱ�ͷų�a kJ����,��д�����������Ҵ�ȼ�յ��Ȼ�ѧ��Ӧ����ʽ:����
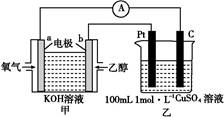
(2)��CO2��H2�ϳ��Ҵ��Ļ�ѧ����ʽΪ2CO2(g)+6H2(g) CH3CH2OH(g)+3H2O(g)��ʵ�����¶ȶԷ�Ӧ��Ӱ����ͼ��ʾ��
CH3CH2OH(g)+3H2O(g)��ʵ�����¶ȶԷ�Ӧ��Ӱ����ͼ��ʾ��
������Ӧ�Ħ�H������0(���������<����=��);
�ڸ÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=�� ��
(3)���ڸû�ѧƽ��,Ϊ�����H2��ת����,�ɲ�ȡ�Ĵ�ʩ����������
| A������ | B����ѹ |
| C���Ӵ��� | D������CO2��Ũ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com