
| ���� | ��ʼ���� | ��ȫ���� |
| Fe��OH��3 | 2.7 | 3.7 |
| Fe��OH��2 | 7.6 | 9.6 |
| Mn��OH��2 | 8.3 | 9.8 |
| Mg��OH��2 | 9.6 | 11.1 |
| Al��OH��3 | 3.7 | 5.7 |
| ��ʼ�ܽ⣺7.8 | ��ȫ�ܽ⣺10.0 |
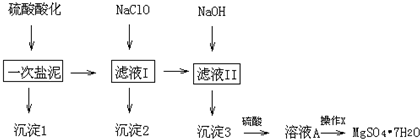
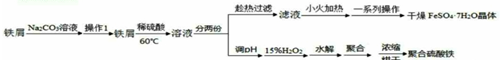
���� һ�������к���þ���ơ����������̵Ĺ����κ�̼���εȳɷ֣��������ᷴӦ��������þ������ƣ����������������������̣����̼���κ�����ת��Ϊ����ˮ�������Σ��õ��ij���1��ҪΪH2SiO3��CaSO4�����ˣ���Һ�������������Ϊ������������Ϊ�������̣�ͬʱ��Һ��Fe3+��Al3+ˮ������Fe��OH��3��Al��OH��3���������Գ���2ΪMnO2��Fe��OH��3��Al��OH��3�����ˣ�����Һ�м���������������������þ���������Գ���3ΪMg��OH��2��������þ�м�������õ�����þ��Һ������Һ��������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����Ȳ��������MgSO4•7H2O���壬
��1����H2SO4������ҺPH��1��2��H2SO4�����ǰ������к���þ���ơ����������̵Ĺ����κ�̼���εȳɷ�ת��Ϊ����������ˮ������ơ����������
��2�����ݸ������ܽ��ijɷַ�����֪������Ӧ��Fe��OH��3��Al��OH��3������������ԭ��Ӧ��ʧ������ȣ��������ӷ���ʽ����ƽ������д��Ӧ�����ӷ���ʽ��
��3������Fe3+������KSCN��Һ����Ѫ��ɫ�����ʼ��飻
��4��������Һ�еõ����ʾ���ķ��������жϣ�����X�Ǵ�����þ��Һ�еõ�MgSO4•7H2O���壬��Ҫ����Ũ����Һ����ȴ�ᾧ��ϴ�Ӹ��
��5��AΪ����þ��Һ�������Һ����������Һ������������ʧ���ӷ���������Ӧ��
��6����������������غ����õ�����þ��������ʵ�����������������Ʒ���ȣ�
��� �⣺��1�������к���þ���ơ����������̵Ĺ����κ�̼���εȳɷ֣���H2SO4������ҺPH��1��2�����̼���κ�����ת��Ϊ����ˮ�������Σ��Ѹ������γ�����Ƴ������ѹ���������γɹ���������˳�ȥ��
�ʴ�Ϊ���������е�̼���κ�����ת��Ϊ�����Ե������Σ�ͬʱ��������ƺ����ȥ��
��2���������ᷴӦ��������þ�������������������������������Ϊ������������Ϊ�������̣�������ҺPH��Fe3+��Al3+ˮ������Fe��OH��3��Al��OH��3������NaClO��Һ�ڼ��������½���Һ�е�Mn2+������MnO2����Ӧ�����ӷ���ʽΪMn2++ClO-+H2O=MnO2��+2H++Cl-�������ˮ��Ϊ���ȷ�Ӧ������������Al3+��Fe3+ˮ���Լ�Mn2+������MnO2��
�ʴ�Ϊ��Fe��OH��3��Al��OH��3��Mn2++ClO-+H2O=MnO2��+2H++Cl-��
��3��Fe3+������KSCN��Һ����Ѫ��ɫ��Fe��SCN��3�������ø÷�Ӧ���м��飬
�ʴ�Ϊ��ȡ����II�����Һ1��2 ml���Թ��У���������KSCN��Һ�������Һ���Ժ�ɫ��֤����Һ����Fe3+��
��4������X�Ǵ�����þ��Һ�еõ�MgSO4•7H2O���壬��Ҫ����Ũ����Һ����ȴ�ᾧ��ϴ�Ӹ��
�ʴ�Ϊ������Ũ���������ᾧ��
��5��AΪ����þ��������Һ�������Һ����������Һ������������ʧ���ӷ���������Ӧ��������Һ�е�ⷴӦΪ��2H2O-4e-=O2��+4H+�������ҺA���ܵõ�����Mg��
�ʴ�Ϊ�����ܣ� 2H2O-4e-=O2��+4H+��
��6��ȷ�����Ƶõ���Ʒ5g����200mLˮ�ܽ⣬����2mol•L-1������5mL���ڲ��Ͻ����µμ�����2mol•L-1 BaCl2��Һ����ַ�Ӧ�ó���4.66g��
���ɳ���BaSO4���ʵ���=$\frac{4.66g}{233g/mol}$=0.02mol��
MgSO4•7H2O���ʵ���Ϊ0.02mol������=0.02mol��246g/mol=4.92g��
��Ʒ����=$\frac{4.92g}{5g}$��100%=98.4%��
�ʴ�Ϊ��98.4%��
���� ���⿼�����ʵ��Ʊ������ӣ��漰���ʵļ����Լ�������ת����֪ʶ����Ŀ��Ϊ�ۺϣ��Ѷ��еȣ�����ע��Ҫ��������������ݣ�����ѧ���ķ���������


 �Ƹ�С״Ԫ�������������ϵ�д�
�Ƹ�С״Ԫ�������������ϵ�д� ����һ������ܼƻ�ϵ�д�
����һ������ܼƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
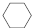 ��g��$?_{����}^{Pt-Sn/Al_{2}O_{3}}$
��g��$?_{����}^{Pt-Sn/Al_{2}O_{3}}$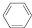 ��g��+3H2��g����
��g��+3H2��g����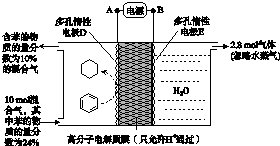
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
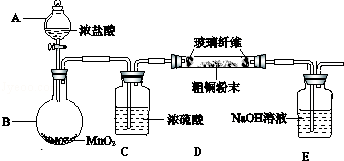
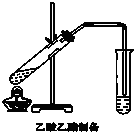 ��1��Ϊ�˼���ͳ�ȥ���еĸ������ʣ��������Ϊ���ʣ�����Ӣ���ѡ���ʵ��ļ����Լ����Ӣ���ѡ���ʵ��ij����Լ�������ѡ�Ĵ�����ĸ������Ӧ�Ŀո��ڣ�
��1��Ϊ�˼���ͳ�ȥ���еĸ������ʣ��������Ϊ���ʣ�����Ӣ���ѡ���ʵ��ļ����Լ����Ӣ���ѡ���ʵ��ij����Լ�������ѡ�Ĵ�����ĸ������Ӧ�Ŀո��ڣ�| ���� | �����Լ� | �����Լ� |
| ���飨��ϩ�� | ||
| �ƾ���ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �ö������ȣ�ClO2�����������ƣ�Na2FeO4�������;�ˮ�������ͳ�ľ�ˮ��Cl2�Ե�ˮ���������dz�������ˮ�����¼�����ClO2��Na2FeO4��ˮ���������зֱ𱻻�ԭΪCl-��Fe3+��
�ö������ȣ�ClO2�����������ƣ�Na2FeO4�������;�ˮ�������ͳ�ľ�ˮ��Cl2�Ե�ˮ���������dz�������ˮ�����¼�����ClO2��Na2FeO4��ˮ���������зֱ𱻻�ԭΪCl-��Fe3+���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
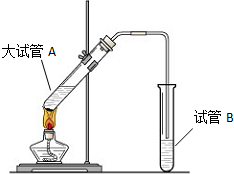 �����dzµ��㡱��������Ϊ���ڴ������������������ζ��������������ʵ��������Ҳ��������ͼ��ʾ��װ����ȡ�����������ش��������⣺
�����dzµ��㡱��������Ϊ���ڴ������������������ζ��������������ʵ��������Ҳ��������ͼ��ʾ��װ����ȡ�����������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | CO2 | B�� | HCl | C�� | BaSO4 | D�� | NaOH��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ӦZ2+2A2+�T2A3++2Z-���Խ��� | |
| B�� | ZԪ���ڷ�Ӧ���б���ԭ���ڷ�Ӧ���б����� | |
| C�� | ��������ǿ������˳����XO4-��Z2��B2��A3+ | |
| D�� | ��ԭ����ǿ������˳����Z-��B-��A2+��X2+ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com