
| m |
| M |
| V |
| Vm |
| m |
| M |
| m | ||
|
| V |
| Vm |
| 4.48L |
| 22.4L/mol |
| 24g |
| 32g/mol |
| m | ||
|
| 8.5 | ||
|



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��XΪ�ǵ���� |
| B��X��������� |
| C��X��ǿ����� |
| D��X�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
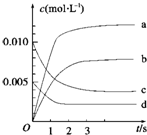 ��2L���ܱ������ڣ�800��ʱ��Ӧ2NO��g��+O2��g��?2NO2��g����ϵ�У�n��NO����ʱ��ı仯�����
��2L���ܱ������ڣ�800��ʱ��Ӧ2NO��g��+O2��g��?2NO2��g����ϵ�У�n��NO����ʱ��ı仯�����| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| n��NO����mol�� | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������Ħ��������63g |
| B��1mol CO��������28g |
| C��4g������Ӧ��Ħ��������2 g������Ӧ��Ħ��������2�� |
| D������Ħ����������ֵ�ϵ�����ԭ�ӵ����ԭ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ԫ������Ȼ���м�������̬�����л���̬ |
| B����������Ⱦ��ũ�P��������ʯ��ʯ��ĩ��������Σ�� |
| C����鲡��θ�����õı��ͣ��ȿ�����BaSO4��Ҳ������BaCO3 |
| D��SO2��SO3��Ϊ���������������ˮ��Ӧ������Ӧ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� |
| H2O |
| NaOH(aq) |
| ϡH2SO4 |
| ���������� |
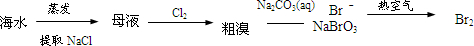
| A���٢ۢ� | B���ڢۢ� |
| C���ڢܢ� | D���٢ܢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com