
【题目】H2SO3水溶液中存在电离平衡H2SO3![]() H++ HSO3- 和HSO3-
H++ HSO3- 和HSO3-![]() H++ SO32-,若对H2SO3溶液进行如下操作,则结论正确的是:( )
H++ SO32-,若对H2SO3溶液进行如下操作,则结论正确的是:( )
A.通入氯气,溶液中氢离子浓度增大
B.通入过量H2S,反应后溶液pH减小
C.加入氢氧化钠溶液,平衡向右移动,pH变小
D.加入氯化钡溶液,平衡向右移动,会产生亚硫酸钡沉淀
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是
A.向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中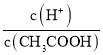 减小
减小
B.CH3COONa溶液从20℃升温至30℃,溶液中![]() 增大
增大
C.向0.1 mol·L-1氨水中加入少量硫酸铵固体,溶液中![]() 增大
增大
D.向AgCl、AgBr的饱和溶液中加入少量硝酸银,溶液中![]() 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温、催化剂条件下,某反应达到平衡,平衡常数K=![]() 恒容时,温度升高,H2浓度减小.下列说法正确的是( )
恒容时,温度升高,H2浓度减小.下列说法正确的是( )
A. 该反应的焓变为负值
B. 2CO2(g)+2H2(g)2CO(g)+2H2O(g) 的平衡常数K1=K2
C. 升高温度,正反应速率增大,逆反应速率减小,平衡正向移动
D. 若恒容、恒温下充入CO,则K值变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是重要的化工基础原料。用乙烯合成光学树脂CR-39单体的过程如下:
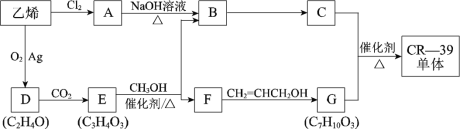
已知:i.CR-39单体结构简式是:
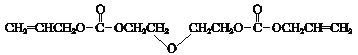
ii.酯与醇有如下反应:![]()
(1)乙烯转化为A的反应类型是___________。
(2)在D、E的分子中,都只有一种化学环境的氢原子。 D的结构简式是__________。E为五元环状化合物,E与CH3OH反应的化学方程式是_____________。
(3)G与足量NaOH溶液反应的化学方程式是________________。
(4)F的一种同分异构体K,其分子中不同化学环境的氢原子个数比是3∶1∶1∶1,且能与NaHCO3反应。
①K能发生消去反应,生成的有机物的结构简式是______________ 。
②K在一定条件下合成高分子化合物的化学方程式是_______________。
(5)下列有关C的叙述正确的是(填写序号)_______。
a. 能与乙酸发生酯化反应 b. 能与乙醇发生酯化反应
c. 1 mol C最多能与2 mol Na反应 d. C的同分异构体不能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出或完成下列热化学方程式。
(1)0.5molCH4完全燃烧生成CO2和液态水时,放出445kJ 的热量。写出CH4燃烧的热化学方程式__________。
(2)通常人们把拆开1mol某化学键吸收的能量看成该化学键的键能。下表是一些化学键的键能。
化学键 | C-H | C-F | H-F | F-F |
键能kJ/mol | 414 | 489 | 565 | 155 |
根据键能数据估算下列反应:CH4(g) + 4F2(g)=CF4(g) + 4HF(g)的反应热△H为_____。
(3)1840年瑞士的化学家盖斯(Hess)在总结大量实验事实(热化学实验数据)的基础上提出:“定压或定容条件下的任意化学反应,在不做其它功时,不论是一步完成的还是几步完成的,其热效应总是相同的(反应热的总值相等)。”
已知:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ΔH1
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) ΔH2
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) ΔH3
请写出CO还原FeO的热化学方程式:______。
(4)在101KP下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题:
①氢气的燃烧热为__________;
②氢气燃烧热的热化学方程式为________;
(5)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2;
Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s) ΔH3=+84.6kJ·mol-1。
则ΔH2=_______kJ·mol-1;
(6)白磷与氧气可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为P—P a kJ·mol-1、P—O b kJ·mol-1、P=O c kJ·mol-1、O=O d kJ·mol-1。根据图示的分子结构和有关数据估算该反应的ΔH为_____。
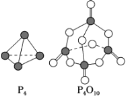
(7)同素异形体相互转化的反应热相当小而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的”观点来计算反应热。已知:
①P4(白磷,s)+5O2(g)=P4O10(s) ΔH1=-2 983.2 kJ·mol-1
②P(红磷,s)+5/4O2(g)=1/4P4O10(s) ΔH2=-738.5 kJ·mol-1
相同状况下,能量较低的是________;白磷的稳定性比红磷________(填“大”或“小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种集强氧化性、吸附、絮凝于一体的新型多功能处理剂,其生产工艺如图所示:
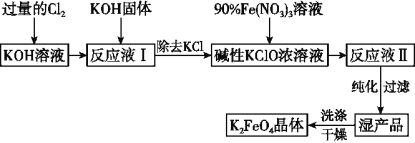
已知K2FeO4具有下列性质:
①可溶于水、微溶于浓KOH溶液
②在0~5 ℃、强碱性溶液中比较稳定
③在Fe3+和Fe(OH)3催化作用下发生分解
④在酸性至碱性条件下,能与水反应生成Fe(OH)3和O2
请完成下列填空:
(1)已知Cl2与KOH在较高温度下反应生成KClO3。在不改变KOH溶液的浓度和体积的条件下,生产KClO应在温度___________的情况下进行(填“较高”或“较低”)。
(2)生产K2FeO4的反应原理是:Fe(NO3)3+KClO+KOH→K2FeO4+KNO3+KCl+H2O(未配平),则该反应中氧化剂与还原剂的物质的量之比为______________。
(3)K2FeO4在弱碱性条件下能与水反应生成Fe(OH)3和O2,则该反应的化学方程式为________________。
(4)在“反应液Ⅰ”中加KOH固体的目的是___________。
A. 为下一步反应提供反应物
B. 与“反应液Ⅰ”中过量的Cl2继续反应,生成更多的KClO
C. KOH固体溶解时会放出较多的热量,有利于提高反应速率
D. 使副产物KClO3转化为KCl
(5)制备K2FeO4时,须将90%的Fe(NO3)3溶液缓慢滴加到碱性的KClO浓溶液中,并且不断搅拌。采用这种混合方式的原因是_______________________ (答出1条即可)。
(6)从“反应液Ⅱ”中分离出K2FeO4晶体后,可以得到的副产品有________ (写化学式)。
(7)工业上常用“间接碘量法”测定高铁酸钾样品中高铁酸钾的含量,其方法是:用碱性的碘化钾溶液(pH为11~12)溶解3.96 g高铁酸钾样品,调节pH为1,避光放置40分钟至反应完全(高铁酸根离子全部被还原成铁离子),再调节pH为3~4(弱酸性)。以1.0 mol/L的硫代硫酸钠标准溶液为滴定剂进行滴定(2Na2S2O3+I2=Na2S4O6+2NaI),当达到滴定终点时,用去硫代硫酸钠标准溶液15.00 mL,则原高铁酸钾样品中高铁酸钾的质量分数为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从宏观现象探究微观本质是重要的化学学科素养。以亚硫酸纳(Na2SO3)为实验对象,探究其性质。实验如下:
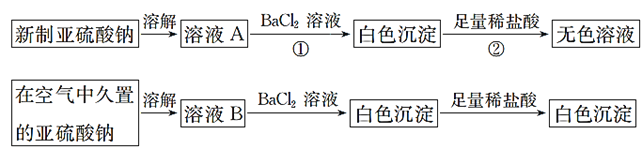
(1)写出上述实验中②的离子方程式:__________。
(2)通过上述实验可知,在空气中久置的亚硫酸纳固体中会混有____________ (填化学式)。
(3)亚硫酸纳晶体样品若变质,下列说法错误的是 _______________。
A.晶体表面变黄 B.其水溶液pH 将减小 C.其样品质量将增加
(4)将碳酸纳溶液加热到40 ℃通入二氧化硫饱和后,再加入等量的碳酸钠溶液,在避免与空气接触的情况下结晶可制得亚硫酸钠,该制备过程总反应的化学方程式 ___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温,不同pH下,Fe(OH)3(s)与Cu(OH)2(s)分别在溶液中达到溶解平衡时,金属阳离子浓度随pH的变化如图所示。下列判断正确的是
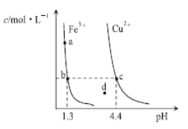
A.加适量盐酸可使溶液中c(Fe3+)由a点变到b点
B.c、d两点代表的溶液中,c(H+) c(OH-)不相等
C.a、b两点时,Fe(OH)3在溶液中均达到饱和
D.Ksp[Fe(OH)3] >Ksp[Cu(OH)2]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com