
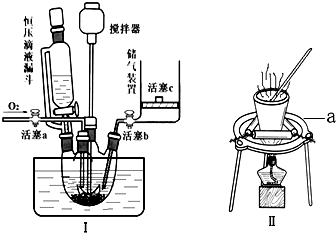
分析 将4.5g铜屑在坩埚中灼烧生成CuO,冷却后将氧化了的铜屑放入装置Ⅰ的四口烧瓶中,再加入25mL3mol•L-1硫酸,同时利用恒压滴液漏斗缓慢、分批加入7mL12mol•L-1硝酸,同时缓缓通入氧气,在水浴加热反应完全,利用储气装置收集氮氧化合物,最后向四口烧瓶中加水溶解,并将溶液转移至烧杯,经蒸发、冷却、过滤、洗涤、干燥得到五水硫酸铜晶体;
(1)图Ⅱ装置中坩埚应放置在三脚架上加热;
(2)检验装置气密性的常见方法是液压法或气压法,装置I的气密性ρ检查首先要形成一个密闭系统,再利用活塞C的移动来检查判断;
(3)当其中一种反应物完全反应掉说明反应完全,可根据铜屑固体的减小来判断反应进行的程度;
(4)储气装置除了储气和储液作用以外,通过活塞的移动,改变储气装置体积的变化,调整装置I内的气体压强;85℃到90℃水浴加热蒸馏,收集到的应该是沸点低于水浴温度的液体,可分析反应物中硝酸易挥发、硫酸是高沸点酸即可判断;
(5)为了提高五水硫酸铜晶体的纯度,需要除去混有的少量硝酸铜晶体,结合除杂原则,可向溶液里引入SO42-;
(6)滴定管水洗后,需要用标准溶液润洗,且要重复操作2~3次;淀粉溶液为指示剂,当最后一滴Na2S2O3溶液滴入时,溶液蓝色褪去,半分钟颜色不变,说明滴定到达终点.
解答 解:将4.5g铜屑在坩埚中灼烧生成CuO,冷却后将氧化了的铜屑放入装置Ⅰ的四口烧瓶中,再加入25mL3mol•L-1硫酸,同时利用恒压滴液漏斗缓慢、分批加入7mL12mol•L-1硝酸,同时缓缓通入氧气,在水浴加热反应完全,利用储气装置收集氮氧化合物,最后向四口烧瓶中加水溶解,并将溶液转移至烧杯,经蒸发、冷却、过滤、洗涤、干燥得到五水硫酸铜晶体;(1)图Ⅱ装置中仪器a为三脚架,故答案为:三脚架;
(2)检查装置Ⅰ气密性的操作方法是关闭活塞a,打开活塞b,向外拉动(或向下推动)活塞c,若一段时间后活塞c恢复至原位,说明气密性良好,故答案为:关闭活塞a,打开活塞b,向外拉动(或向下推动)活塞c,若一段时间后活塞c恢复至原位,说明气密性良好;
(3)随着反应的进行,铜屑固体体积不断减少,当铜屑完全溶解时可判断反应完全,故答案为:铜屑全部溶解;
(4)储气装置除了储气和储液作用以外,还可以通过容器的体积变化来调整装置I内气体压强,达到平衡气压的作用;因硝酸是易挥发性酸,则步骤⑤中蒸馏回收的溶液的溶质主要是硝酸,故答案为:平衡气压;HNO3;
(5)通过加入稀硫酸并结合加热蒸馏除去少量硝酸铜晶体,提高五水硫酸铜晶体的纯度,故答案为:B;
(6)滴定管水洗后,润洗操作是往滴定管中注入少量待装液,倾斜滴定管,小心转动,使待装液润湿整支滴定管内壁,把液体从滴定管尖嘴处放出,重复2到3次;淀粉溶液为指示剂,当最后一滴Na2S2O3溶液滴入时,I2与Na2S2O3恰好反应,I2被完全消耗,溶液蓝色褪去,半分钟颜色不变,说明滴定到达终点,
故答案为:往滴定管中注入少量待装液,倾斜滴定管,小心转动,使待装液润湿整支滴定管内壁,把液体从滴定管尖嘴处放出,重复2到3次;由蓝色刚好变为无色.
点评 本题以硫酸铜晶体制备为载体,考查实验的基本操作及混合物的分离提纯,涉及装置气密性检查、蒸馏、滴定实验等,考查学生分析实验的能力和数据处理及计算能力,难度中等,要求学生要有扎实的基础知识和灵活应用知识解决问题的能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 水溶液导电的一定是分子晶体 | B. | 熔融态导电的一定是离子晶体 | ||
| C. | 原子晶体固态一定不导电 | D. | 分子晶体熔融态一定不导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 能使潮湿的有色布条褪色 | |
| B. | 钠在氯气中燃烧,生成白色的烟 | |
| C. | 纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现白色烟雾 | |
| D. | 氯气能与水反应生成次氯酸和盐酸,久置氯水最终变为稀盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 举行“地球一小时”熄灯活动 | B. | 露天焚烧稻草和秸秆 | ||
| C. | 夏天将空调的温度设置在26℃以上 | D. | 生活垃圾分类回收处理 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
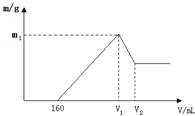 将镁铝的混合物0.1mol溶于100mL2mol/L硫酸溶液中,然后再滴加1mol/L氢氧化钠溶液,请回答以下问题:
将镁铝的混合物0.1mol溶于100mL2mol/L硫酸溶液中,然后再滴加1mol/L氢氧化钠溶液,请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com