
����Ŀ�����ֶ���������Ԫ�� X��Y��Z��W �����λ�������Ԫ�� X ��ԭ�Ӻ���������� Z�� 2 ��������˵������ȷ����

A. W Ԫ�صļ���̬�⻯������ȶ��Ա� Z Ԫ�صļ� ����̬�⻯��ĸ�
B. �������(ZW)2 �ĽṹʽΪ N��C��C��N
C. X��Y��W ����Ԫ�صļ����Ӱ뾶������ Y
D. Ԫ�� X λ�����ڱ��е������ڡ�����A�壬�䵥���Ʊ����õ������ XCl2 �ķ�����
���𰸡�C
��������Ԫ��X��ԭ�Ӻ����������Z��2��������Z�ĺ��������Ϊx����XΪx+8-2�����x+8-2=2x�����x=6����XΪMg��YΪAl��ZΪC��WΪN��A. Ԫ�صķǽ�����Խǿ������̬�⻯��Խ�ȶ���WԪ�صļ���̬�⻯������ȶ��Ա�ZԪ�صļ���̬�⻯��ĸߣ���A��ȷ��B. ����8�����ȶ��ṹ��Nԭ����Ҫ�γ�3�����õ��Ӷԣ�Cԭ����Ҫ�γ�4�����õ��Ӷԣ� (CN)2�ĽṹʽΪN��C��C��N����B��ȷ��C. X��Y��W����Ԫ�صļ����Ӿ�����ͬ�ĵ��Ӳ�ṹ���˵����Խ�����Ӱ뾶ԽС���뾶������W����C����D. þΪ12��Ԫ�أ�λ�����ڱ��е������ڡ��ڢ�A�壬��ҵ�ϳ��õ�����ڵ��Ȼ�þ�ķ���ұ������þ����D��ȷ����ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�Ȼ�ѧ����ʽ��
H2O(g)=H2(g)+![]() O2(g)��H=+241.8kJ��mol-1
O2(g)��H=+241.8kJ��mol-1
H2(g)+![]() O2(g)=H2O��1����H=��285.8kJ��mol-1
O2(g)=H2O��1����H=��285.8kJ��mol-1
��1gҺ̬ˮ��Ϊˮ����ʱ���������仯��( )
A������88kJ B������44 kJ C������44kJ D������2.44 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֹ����к������гɷ֣�

��֪����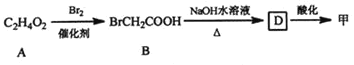
C2H4O2![]() BrCH2COOH
BrCH2COOH![]() D
D![]() ��
��
��1mol������NaHCO3�����ʵ����Ǽ�2��
��
�ش��������⣺
(1)������֪�ٵõ���
�ټ��к��в����ͼ��Ĺ���������Ϊ______��
��A��BΪȡ����Ӧ��A�Ľṹ��ʽΪ______��
��B��D�Ļ�ѧ����ʽΪ______��
(2)����һ��������������״�����л��߷��ӻ�����Ļ�ѧ����ʽΪ______��
(3)�ɱ�������;���ɵ�һ����Ҫ��ҽҩ�������м���J(���ַ�Ӧ������ȥ)��

���û�ѧ������ȥE�в�����������(����ʱE�ͱ���Һ̬������������ˮ�е��ܽ�)����1�������Լ�������Ϊ______ ����2��3�����ֱ��ǹ��ˡ���Һ��
�ھ�E��G��H�����Ĺ�������______�����Ա����л��������д��ں��ֹ����ŵ�������______��
��J��ͬ���칹�����ں˴Ź�����������ʾΪ����壬�������Ϊ3��2����״�Ҳ�����֧�����칹�干��______ ��(���������칹)������ij�칹��L�еĹ����Ŷ�����H2�����ӳɷ�Ӧ����L�Ľṹ��ʽΪ______ (ֻдһ��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��F��G��H ��Ԫ�����ڱ�ǰ�����ڳ���Ԫ�أ���ԭ���������������������Ϣ���±���
Ԫ�� | �����Ϣ |
A | ԭ�Ӻ����� 6 �ֲ�ͬ�˶�״̬�ĵ��� |
C | ��̬ԭ���� s ����������p ����������� |
D | ԭ�Ӱ뾶��ͬ����Ԫ������� |
E | ��̬ԭ�����������Ų�ʽΪ 3s23p1 |
F | ��̬ԭ�ӵ������ p ������������ӵ������������������ӵ��� �������෴ |
G | ��̬ԭ�Ӻ����� 7 ���ܼ���������ߵ��ܼ����� 6 ������ |
H | ���ҹ�ʹ������ĺϽ��е�����Ҫ����Ԫ�� |
(1) A Ԫ�ص�������_______________��A Ԫ�غ� F Ԫ���γɵ��������ķ��ӹ���Ϊ_______________���÷�����_______________���ӡ������������������Ǽ�������
(2) B Ԫ���γɵĵ��ʷ�����������������Ŀ֮��Ϊ_______________��
(3) G Ԫ�صĵͼ������ӵ����ӽṹʾ��ͼ��_______________��
(4) G �ĸ������ӵ���Һ�� H ���ʷ�Ӧ�����ӷ���ʽΪ___________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ե����仯������о�������Ҫ���塣
(1)����2NO(g)+O2(g) ![]() 2NO2(g)��Ӧ��������������Ԫ��Ӧ��
2NO2(g)��Ӧ��������������Ԫ��Ӧ��
�� 2NO(g) ![]() N2O2(g)(��) ��H1��0 ����1��=k1��c2(NO)����1��=k1��c(N2O2)��
N2O2(g)(��) ��H1��0 ����1��=k1��c2(NO)����1��=k1��c(N2O2)��
�� N2O2(g)+O2(g) ![]() 2NO2(g)(��) ��H2��0����2��=k2��c(N2O2)c(O2)����2��=k2��c2(NO2)������2NO(g)+O2(g)
2NO2(g)(��) ��H2��0����2��=k2��c(N2O2)c(O2)����2��=k2��c2(NO2)������2NO(g)+O2(g) ![]() 2NO2(g)��Ӧ���ʿ����Ļ�Ԫ��Ӧ��________(����)��һ�������£���Ӧ2NO(g)+O2(g)
2NO2(g)��Ӧ���ʿ����Ļ�Ԫ��Ӧ��________(����)��һ�������£���Ӧ2NO(g)+O2(g) ![]() 2NO2(g)�ﵽƽ��״̬��ƽ�ⳣ��K��_______(�ú���k1����k1����k2����k2�� �Ĵ���ʽ��ʾ)
2NO2(g)�ﵽƽ��״̬��ƽ�ⳣ��K��_______(�ú���k1����k1����k2����k2�� �Ĵ���ʽ��ʾ)
(2)ʹ��SNCR��������������ӦΪ��
4NH3(g)+4NO(g)+O2(g) ![]() 4N2(g)+6H2O(g) ��H��0
4N2(g)+6H2O(g) ��H��0
����Ӧ��4NH3(g)+4O2 (g) ![]() 2N2O (g)+6H2O (g) ��H��0
2N2O (g)+6H2O (g) ��H��0
�±����ܱ���ϵ�н���ʵ�飬��ʼͶ��һ����NH3��NO��O2���ⶨ��ͬ�¶��£�����ͬʱ���ڸ���ֵ�Ũ�ȡ�

N2Ũ�ȱ仯����___________________���Խ���ԭ��______________________��
���ݱ��������Ʋ⣬����Ӧ��ʼ�������¶�������_____________________��

(3)��������ȼ�ϵ��ԭ���о������°��ĺϳɣ���ع���ʱMV2+/MV+�ڵ缫��ø֮�䴫�ݵ��ӣ�ʾ��ͼ������ʾ����д�������ڹ̵�ø�����·����Ļ�ѧ��Ӧ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ������ѧϰ��ѧ����Ҫ���ߣ�����˵����ȷ����(����)
A.���⻯����Һ�����ˮ��ƽ�� HS-+H2O![]() H3O��+S2-
H3O��+S2-
B.���������绯ѧ��ʴ�ĸ�����ӦʽΪ��Fe-3e-=Fe3+
C.��֪�����ȼ����Ϊ890.3 kJ��mol-1�������ȼ���ȵ��Ȼ�ѧ����ʽ�ɱ�ʾΪCH4(g)+2O2(g)=CO2(g)+2H2O(g)����H=-890.3 kJ��mol��1
D.��0.1 mol��L��1HA��Һ��pH=3������֪NaA��Һ����A-+H2O![]() HA+OH-
HA+OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йذ����ӵ�����NA�������в���ȷ���ǣ� ��
A.1mol NaHSO4������������������ĿΪNA
B.���³�ѹ�£�92 g��NO2��N2O4������庬�е�ԭ����Ϊ6NA
C.��״���£�22.4L HF���е�����Ϊ8NA
D.60gʯӢ�����к��е�Si-O����ĿΪ4NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1,4-��������(![]() )��һ�ֳ������ܼ���������ͨ�����з����Ƶ���ͼ��ʾ������A��
)��һ�ֳ������ܼ���������ͨ�����з����Ƶ���ͼ��ʾ������A��
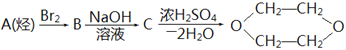
A. 1-��ϩ B. 1,3-����ϩ C. ��Ȳ D. ��ϩ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com