
科目:高中化学 来源: 题型:
下列不能说明化学具有创造性和实用性的是( )
A.化学家哈伯用催化法合成氨后,德国就能生产硝酸
B.科学家们合成碳纳米管,用作分子导线和超小型的电子器件
C.俄国科学家门捷列夫发现元素周期律
D.诺贝尔用硝化甘油制成了炸药,并用于工业生产
查看答案和解析>>
科目:高中化学 来源: 题型:
下面是一些排列无序的物质,请将下列各物质填写到下列树状分类法图中相应的位置上:Cu、H2、NaCl溶液、CaO、H2O、Hg、S、Ca(OH)2、H2SO4、CaCO3、NH3·H2O、CH3COOH


查看答案和解析>>
科目:高中化学 来源: 题型:
反应Fe(s)+CO2(g) 
 FeO(s)+CO(g),700 ℃时平衡常数为1.47,900 ℃时平衡常数为2.15。下列说法正确的是 ( )
FeO(s)+CO(g),700 ℃时平衡常数为1.47,900 ℃时平衡常数为2.15。下列说法正确的是 ( )
A.升高温度该反应的正反应速率增大,逆反应速率减小
B.该反应的化学平衡常数表达式为K=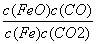
C.该反应的正反应是吸热反应
D.增大CO2浓度,平衡常数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
利用右图装置测定中和热的实验步骤如下:
①用量筒量取50 mL 0.25 mol·L-1硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50 mL 0.55 mol·L-1NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度。
回答下列问题:
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3 kJ·mol-1):____________________________________________________________________。
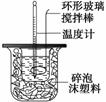 (2)倒入NaOH溶液的正确操作是__________(从下列选项中选出)。
(2)倒入NaOH溶液的正确操作是__________(从下列选项中选出)。
A.沿玻璃棒缓慢倒入B.分三次少量倒入C.一次迅速倒入
(3)使硫酸与NaOH溶液混合均匀的正确操作是________(从下列选项中选出)。
A.用温度计小心搅拌
B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(4)实验数据如下表:
①请填写下表中的空白:
| 温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 |
|
| 2 | 27.0 | 27.4 | 27.2 | 32.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 | |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 |
②近似认为0.55 mol·L-1NaOH溶液和0.25 mol·L-1硫酸溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18 J·g-1·℃-1。依据上表数据计算中和热ΔH=________(取小数点后一位)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应所产生的气体体积在标准状况下为22.4 L的是( )
A.将2 mol金属Cu与含2 mol H2SO4的浓硫酸共热
B.将27 g Al与足量 盐酸反应
盐酸反应
C.常温下,将18 g金属铝投入足量NaOH溶液中
D.常温下,将10.8 g Al和22.4 g Fe投入到300 g 98%的硫酸中
查看答案和解析>>
科目:高中化学 来源: 题型:
某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等。有人设计了图中的工艺流程,利用常用的酸、碱 和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。
和工业生产中的废铁屑,从废水中回收金,并生产一定量的铁红和氧化铜。
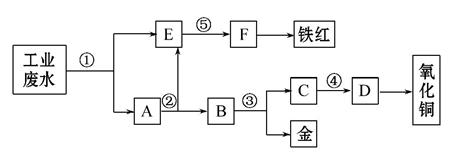
填写下面空白:
(1)图中标号处需加入的相应物质分别是
①________、②________、③________、④________、⑤________;
(2)写出①处的离子方程式:________________________ _______________;
_______________;
写出③处的化学方程式:__________________________________________;
(3)铁红的化学式为________;分别写出铁红和氧化铜在工业上的一种主要用途
 :铁红________;氧化铜________。
:铁红________;氧化铜________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学式与指定物质的主要成分对应正确的是
A.CH4——天然气 B.CO2——水煤气
C.CuSO4▪5H2O——明矾 D.NaHCO3——苏打粉
查看答案和解析>>
科目:高中化学 来源: 题型:
I、恒温下,将a mol N2与b mol H2的混合气体通入一个固体容积的密闭容器中,发生如下反应:N2(g)+3H2(g)  2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,nt(N2)=13 mol,nt(NH3)=6 mol,计算 a= 。
(2)反应达到平衡时,混合气体的体积为716.8L(标况下),其中NH3的含量(体积分数)为25%。计算平衡时NH3的物质的量 。。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),
n( 始):n(平)= 。
(4)原混合气体中,a:b= 。
(5)达到平衡时,N2和H2的转化率之比,a(N2):a(H2)= 。
(6)平衡混合气体中,n(N2):n(H2):n(NH3)= 。
II、若向体积不变的密闭容器中充入2 mol N2和6 mol H2,一定条件下发生反应:
N2(g)+ 3 H2(g) 2 NH3(g),平衡时混合气共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
2 NH3(g),平衡时混合气共7 mol.令a、b、c分别代表N2、H2、NH3起始加入的物质的量,维持温度不变,使达到平衡时各成分的百分含量不变.则:
(1)若a=0,b=0,则c= .
(2)若a=0.7,b=2.1,则:
① c= .
②这时反应向 进行,因为: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com