
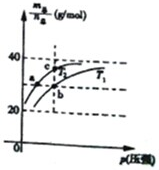
 已知N2O4(g)?2NO2(g)△H>0且平衡体系的总质量(m总)与总物质的量(n总)之比在不同温度下随压强变化曲线如图所示,下列说法正确的是( )
已知N2O4(g)?2NO2(g)△H>0且平衡体系的总质量(m总)与总物质的量(n总)之比在不同温度下随压强变化曲线如图所示,下列说法正确的是( )| A、平衡常数K(a)=K(b)<K(c) | ||
| B、反应速率:va<vb | ||
| C、温度:T2>T1 | ||
D、当
|
| 46x+92y |
| x+y |


科目:高中化学 来源: 题型:
A、CO2分子比例模型: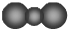 |
B、NH4I的电子式: |
| C、乙烯的结构简式 C2H4 |
D、NaH中氢离子结构示意图为 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸钠溶液呈碱性,可用于清洗油污 |
| B、水与乙醇以任意比例互溶,可用水洗、分液的方法除去溴乙烷中的乙醇 |
| C、镧镍合金能大量吸收H2形成金属氢化物,可作储氢材料 |
| D、游泳池中常加入硫酸铜,其主要作用是铜离子水解生成Cu(OH)2胶体,能吸咐池中的悬浮物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、称取1.06 g 无水碳酸钠,加入100 mL 容量瓶中,加水溶解、定容 |
| B、称取1.06 g 无水碳酸钠,加入蒸馏水,搅拌、溶解,配制100 mL溶液 |
| C、转移Na2CO3溶液时,未用玻璃棒引流,直接倒入容量瓶中 |
| D、定容后,塞好瓶塞,反复倒转,摇匀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
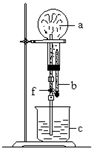 在如图装置中,烧瓶中充满干燥体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出.则a和b不可能是( )
在如图装置中,烧瓶中充满干燥体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出.则a和b不可能是( )| a(干燥气体) | b(液体) | |
| A | NO2 | 水 |
| B | NH3 | 1mol/L盐酸溶液 |
| C | Cl2 | 4mol/L氢氧化钠溶液 |
| D | CO2 | 水 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下的两种溶液:①0.1 mol?L-1 CH3COOH溶液;②0.3 mol?L-1 CH3COOH与0.1 mol?L-1NaOH两溶液等体积混合后,c(H+):①<② |
| B、已知NaHSO3溶液的pH<7,则该溶液中:c(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3) |
| C、相同条件下,pH=9的 ①CH3COONa溶液;②NH3?H2O溶液;③NaOH溶液中,由水电离出的c(OH-):①>②>③ |
| D、等物质的量浓度的CH3COONa与CH3COOH的混合溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等质量的两种盐分别与足量盐酸反应,碳酸钠产生的气体多 |
| B、等质量的两种盐分别与足量盐酸反应,碳酸钠反应更剧烈 |
| C、盐酸滴加到碳酸钠溶液中与碳酸钠溶液滴加到盐酸中,两者的现象相同 |
| D、盐酸滴加到碳酸氢钠溶液中与碳酸氢钠溶液滴加到盐酸中,两者的现象相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、vA=0.15 mol/(L?min) |
| B、B的转化率为20% |
| C、B的平衡浓度是0.5 mol/L |
| D、x值等于2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
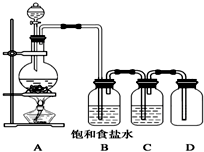 用如图装置制取并收集氯气,试回答下列问题:
用如图装置制取并收集氯气,试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com