
【题目】苯乙酮酸是医药合成中的一种重要中间体,某研究小组对苯乙酮酸展开如下设计研究:

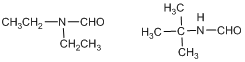
已知:I. ![]() II.
II. ![]()
请回答:
(1)下列说法正确的是_____________;
A.反应①②④都是取代反应 B.化合物C能发生消去反应
C.化合物D中含有两种官能团 D.化合物E的分子式为C17H25NO3
(2)反应④D→E的化学方程式是___________________________________。
(3)化合物M的结构简式是___________________________。
(4)写出同时符合下列条件的化合物 的所有同分异构体的结构简式____________。
的所有同分异构体的结构简式____________。
①能发生银镜反应
②1H-NMR谱显示分子中有三种不同化学环境的氢原子。
(5)采用甲苯为原料制备苯乙酮酸(![]() ),请设计该合成路线(用流程图表示,无机试剂任选)_____。
),请设计该合成路线(用流程图表示,无机试剂任选)_____。
【答案】 BC 
【解析】反应①是指A物质与甲醇在浓硫酸条件下发生酯化反应,故B物质为![]() ;分析B、C的结构可知,反应②(B→C)为加成反应,断裂B中的羰基;分析E的结构简式,逆推D,可知反应③(C→D)为还原反应,C脱氧加氢,羰基被还原,故D的结构简式为:
;分析B、C的结构可知,反应②(B→C)为加成反应,断裂B中的羰基;分析E的结构简式,逆推D,可知反应③(C→D)为还原反应,C脱氧加氢,羰基被还原,故D的结构简式为: ;反应④(D→E)为取代反应,另一种产物为CH3OH。
;反应④(D→E)为取代反应,另一种产物为CH3OH。
(1)A、根据上述分析,只有①④为取代反应,故A错误;B、化合物C含有羟基,连接羟基的碳的有一个邻碳上有H原子,可以发生消去反应,故B正确;C、化合物D的结构简式为 ,含有羟基和酯基两种官能团,故C正确;D、根据E的结构简式,可知E中应含有18个碳原子,故D错误。选BC。
,含有羟基和酯基两种官能团,故C正确;D、根据E的结构简式,可知E中应含有18个碳原子,故D错误。选BC。
(2)D到E为取代反应,另一种产物为CH3OH,所以D→E的化学方程式为:

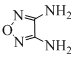
(3)根据已知信息![]() ,C=O与-NH2反应生成H2O,A中含有两个C=O,可以与两个-NH2发生反应,根据F的结构可知,M中有两个-NH2发,所以M的结构简式为:
,C=O与-NH2反应生成H2O,A中含有两个C=O,可以与两个-NH2发生反应,根据F的结构可知,M中有两个-NH2发,所以M的结构简式为: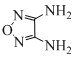 。
。
(4)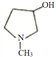 的分子式为C5H11NO,能发生银镜反应,则有-CHO;1H-NMR谱显示分子中有三种不同化学环境的氢原子,即有3种不同位置的H原子,分子比较对称。-CHO上的H是一种等效氢;另外10个H原子处于两个位置,分为三种情况,①N上没有H,有3个对称的-CH3,一个C上有1个H原子;②N上没有H,有2个对称的- CH2CH3,一个C上没有H;③N上有H,还有3个对称的甲基,一个C上没有H。根据上述分析书写,情况①没有对应的结构简式,②③分别有一种,分别为:
的分子式为C5H11NO,能发生银镜反应,则有-CHO;1H-NMR谱显示分子中有三种不同化学环境的氢原子,即有3种不同位置的H原子,分子比较对称。-CHO上的H是一种等效氢;另外10个H原子处于两个位置,分为三种情况,①N上没有H,有3个对称的-CH3,一个C上有1个H原子;②N上没有H,有2个对称的- CH2CH3,一个C上没有H;③N上有H,还有3个对称的甲基,一个C上没有H。根据上述分析书写,情况①没有对应的结构简式,②③分别有一种,分别为: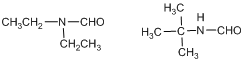 。
。
(5)甲苯为原料制备苯乙酮酸(![]() ),分析碳的骨架可知,要在甲苯的基础上增加一个C原子;根据已知信息II可知,可以用苯甲醛与HCN反应,得
),分析碳的骨架可知,要在甲苯的基础上增加一个C原子;根据已知信息II可知,可以用苯甲醛与HCN反应,得![]() ,在进行催化氧化得到
,在进行催化氧化得到![]() ;所以首先先由
;所以首先先由![]() 得到
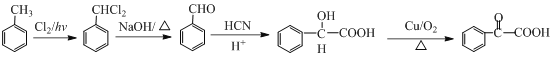
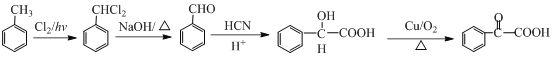
得到![]() ,可以有甲苯与氯气在光照条件下发生取代,得到两个氯原子,氯原子水解得到两个羟基,羟基脱水得醛基。用流程可表示如下:
,可以有甲苯与氯气在光照条件下发生取代,得到两个氯原子,氯原子水解得到两个羟基,羟基脱水得醛基。用流程可表示如下:


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
【题目】实验室配制250mL0.1mol/L的盐酸溶液,填空并请回答下列问题:
(1)配制250mL0.1mol/L的盐酸溶液需要ml容量瓶.还需要 , , . (仪器)
(2)配制时,其正确的操作顺序是计算称量溶解转移定容摇匀装瓶.
(3)若出现如下情况,对所配溶液浓度将有何影响?加蒸馏水时不慎超过了刻度;定容时俯视未冷却 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”,并收集纯净干燥的气体.请回答该实验中的问题.
(1)写出该反应的化学方程式;干燥剂是(写名称).
(2)圆底烧瓶中盛装的水,该装置受热后的主要作用是;烧瓶底部放置了几片碎瓷片,其作用是 .
(3)试管中收集气体是(写化学式),如果要在A处玻璃管处点燃该气体,则必须对该气体进行 . 在虚线框内画出收集该气体的装置图 .(限选仪器:试管、玻璃导管、水槽)
(4)反应后得到黑色固体,主要成分是Fe3O4 , 还含有少量Fe和FeO;限选以下试剂:稀HNO3、稀HCl、KSCN溶液、氯水、CuSO4溶液;
设计实验方案检验所得固体中含有Fe3O4 , 写出实验步骤和实验现象 . 证明固体中含有没完全反应的Fe .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在含有Cu(NO3)2、Mg(NO3)2和AgNO3的溶液中加入适量锌粉,首先置换出的是 ( )
A. Mg B. Cu C. Ag D. H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列物质的关系中不正确的是 ( )
A. 金刚石与石墨互为同素异形体 B. H、 D、T互为同位素
C. CH3-CH3与(CH3)3CH是同系物 D. CH3CH(C2H5)CH3与(CH3)2CHCH2CH3是同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氨可以与灼热的氧化铜反应得到氮气和金属铜:3CuO+2NH3 ![]() 3Cu+N2+3H2O,C中的现象是黑色粉末逐渐变为红色,用示意图中的装置可以实现该反应.
3Cu+N2+3H2O,C中的现象是黑色粉末逐渐变为红色,用示意图中的装置可以实现该反应. 
(1)A中装有Ca(OH)2和NH4Cl混合粉末,该反应的化学方程式是: .
(2)B中加入的是碱石灰,其作用是 .
(3)D中收集到的物质是 , 检验该物质的方法现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知在pH为4~5的溶液中,Cu2+几乎不水解,而Fe3+几乎完全水解。某学生拟用电解CuSO4溶液的方法测定铜的相对原子质量。该同学向pH=3.8酸化的、含有Fe2(SO4)3杂质的CuSO4溶液中加入过量的黑色粉末X,充分搅拌后将滤液用下图所示装置电解,其中某电极增重ag,另一电极上产生标准状况下的气体VmL。下列说法正确的是

A. 铜电极连接电源正极 B. 铜的相对原子质量的计算式是![]()
C. 黑色粉末X是铁粉 D. 石墨电极上发生的反应是4OH--4e-=O2↑+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com