
【题目】完成下列填空:
(1)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸时的反应为:S+2KNO3+3C═K2S+N2↑+3CO2↑.该反应中还原剂是 , 氧化剂是 .
(2)某班同学在玩密室逃脱游戏时,有一个密码锁,需要四个数字的密码开锁,一学生找到一张任务卡如图,则该密码为: 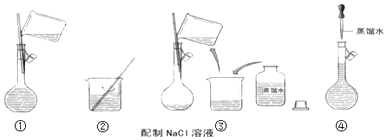
(3)现有下列物质:①Cu ②HCl ③NH3 ④NaCl ⑤CaCO3 ⑥稀硫酸 ⑦NaHSO4 , 其中属于电解质,但熔融状态下并不导电的是(填序号),请写出NaHSO4在水溶液中的电离方程式
(4)写出制备Fe(OH)3胶体的化学方程式 , 向该胶体中逐滴加入稀硫酸的现象为 , 发生反应的离子方程式为
(5)在25℃,101kPa条件下,将15L O2通入10L CO和H2的混合气体中,使其完全燃烧,干燥后,恢复至原来的温度和压强.(1)若剩余气体的体积是15L,则通入10L CO和H2的混合气体中,V(CO)=L,V(H2)=L.若剩余气体的体积为a L,则a的取值范围是 .
【答案】
(1)C;S、KNO3
(2)②③①④
(3)②;NaHSO4=Na++H++SO42﹣
(4)FeCl3+3H2O ![]() ?Fe(OH)3(胶体)+3 HCl;先产生红褐色沉淀,后来沉淀消失;Fe(OH)3+3H+=Fe3++3H2O
?Fe(OH)3(胶体)+3 HCl;先产生红褐色沉淀,后来沉淀消失;Fe(OH)3+3H+=Fe3++3H2O
(5)5;5;10<a<20
【解析】解:(1)反应S+2KNO3+3C═K2S+N2↑+3CO2↑中,S元素化合价由0价降低到﹣2价,则S为氧化剂,N元素化合价由+5价降低到0价,则KNO3为氧化剂,C元素化合价由0价升高到+4价,则C为还原剂,
所以答案是:C;S、KNO3;(2)配制一定物质的量浓度的NaCl溶液步骤为称量、溶解、冷却、移液、洗涤、定容等,所以正确的顺序为:②③①④,
所以答案是:②③①④;(3)①Cu ②HCl ③NH3 ④NaCl ⑤CaCO3 ⑥稀硫酸 ⑦NaHSO4 , 其中属于电解质,但熔融状态下并不导电的物质一定为共价化合物型的电解质,满足体积的有②;
NaHSO4在水溶液中完全电离,其电离方程式为:NaHSO4=Na++H++SO42﹣ ,
所以答案是:②;NaHSO4=Na++H++SO42﹣;(4)将饱和氯化铁溶液加入沸水中加热制备Fe(OH)3胶体,反应的化学方程式为:FeCl3+3H2O ![]() Fe(OH)3(胶体)+3 HCl; 向该胶体中逐滴加入稀硫酸,氢氧化铁胶体先发生聚沉现象生成氢氧化铁沉淀,然后氢氧化铁沉淀与稀硫酸反应生成硫酸铁和水,反应反应为:Fe(OH)3+3H+=Fe3++3H2O,反应现象为:先产生红褐色沉淀,后来沉淀消失,
Fe(OH)3(胶体)+3 HCl; 向该胶体中逐滴加入稀硫酸,氢氧化铁胶体先发生聚沉现象生成氢氧化铁沉淀,然后氢氧化铁沉淀与稀硫酸反应生成硫酸铁和水,反应反应为:Fe(OH)3+3H+=Fe3++3H2O,反应现象为:先产生红褐色沉淀,后来沉淀消失,
所以答案是:FeCl3+3H2O ![]() Fe(OH)3(胶体)+3 HCl;先产生红褐色沉淀,后来沉淀消失;Fe(OH)3+3H+=Fe3++3H2O;(5)设V(CO)为xL,则V(H2)为(10﹣x)L,由
Fe(OH)3(胶体)+3 HCl;先产生红褐色沉淀,后来沉淀消失;Fe(OH)3+3H+=Fe3++3H2O;(5)设V(CO)为xL,则V(H2)为(10﹣x)L,由
2CO+ | O2 |
| 2CO2 | △V |
2 | 1 | 2 | 1 | |
x |
| |||
2H2+ | O2 |
| 2H2O | △V |
2 | 1 | 3 | ||
10﹣x |
|
则 ![]() x+
x+ ![]() (10﹣x)=15+10﹣15,解得:x=5,
(10﹣x)=15+10﹣15,解得:x=5,
即V(CO)=5L,则V(H2)=(10﹣x)L=10L﹣5L=5L,
混合气体中CO与剩余气体体积a之间的关系为: ![]() x+
x+ ![]() (10﹣x)=15+10﹣a,
(10﹣x)=15+10﹣a,
解得:a=10+x,
由于0<x<10,则10<a<20,
所以答案是:5;5;10<a<20.
【考点精析】利用胶体的重要性质和配制一定物质的量浓度的溶液对题目进行判断即可得到答案,需要熟知胶体的性质:①丁达尔现象(可用来鉴别胶体和溶液) ②布朗运动 ③电泳现象 ④胶体聚沉(加入电解质、加入带异种电荷的胶体、加热,均可使胶体聚沉);配制物质的量浓度溶液时,先用烧杯加蒸馏水至容量瓶刻度线1cm~2cm后,再改用交投滴管加水至刻度线.


科目:高中化学 来源: 题型:
【题目】在反应:C+CO2=2CO中,可使反应速率增大的措施是 ( )
①增大压强 ②升高温度 ③通入CO2 ④增加碳的量 ⑤降低压强
A.①②③ B.②③④⑤ C.①②③④ D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一容积为2L的密团容器内加入0.2molN2和0.6molH2,在一定条件下发生如下反应: ![]() N2(g)+
N2(g)+ ![]() H2(g)
H2(g)![]() NH3(g)
NH3(g)
①该反应的平衡常数的表达式是:____________。
②反应中氨气的浓度的变化情况如图所示,计算从反应开始到平衡时,平均反应速率v(H2)=________。
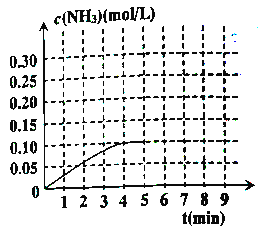
③判断该反应达到平衡状态的标志是_________。
a.N2和NH3浓度相等 b.NH3百分含量保持不变
c.容器中气体的压强保持不变 d.NH3的生成速率与H2的消耗速率相等
e.容器中混合气体的密度保持不变
④反应达平衡后,第5分钟末,保持其它条件不变,仅改变反应温度,则NH3的物质的量浓度不可能为______。
a.0.2mol/L b.0.12mol/L c.0.10mol/L d.0.08mol/L
⑤在第5分钟末,将容器体积缩小一半后,若在第8分钟末达到新平衡(此时NH3浓度约为0.25mol/L),请在上图中画出从第5分钟末开始,再达到新平衡时NH3浓度变化曲线。______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验SO42﹣ , 甲、乙、丙、丁四位同学设计了如下四种方案,其中方案最优的是( )
A.方案甲:试液 ![]() 白色沉淀
白色沉淀 ![]() 沉淀不溶解
沉淀不溶解
B.方案乙:试液 ![]() 无沉淀(也无气泡)
无沉淀(也无气泡) ![]() 白色沉淀
白色沉淀
C.方案丙:试液 ![]() 无沉淀
无沉淀 ![]() 白色沉淀
白色沉淀
D.方案丁:试液 ![]() 白色沉淀(过滤)
白色沉淀(过滤) ![]() 沉淀不溶解
沉淀不溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20种氨基酸的平均相对分子质量为128,假若有一个多肽化合物,由10个氨基酸构成一个肽链,那么该多肽的相对分子质量和至少含有的氨基数目分别是 ( )
A. 1 280,11 B. 1 262,1 C. 1 118,1 D. 1 100,9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与科技、生产、生活密切相关。下列说法正确的是

A.气象环境报告中的“PM2.5”是一种新分子的描述
B.采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量
C.“玉兔号”月球车太阳能电池帆板的材料是二氧化硅
D.如图为雾霾的主要成分示意图,SO2和NxOy都属于酸性氧化物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com