
判断正误,正确的划“√”,错误的划“×”
(1)向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2===2Fe3++2Br2+6Cl- ( )
(2013·海南,10C)
(2)将水蒸气通过灼热的铁粉,铁与水在高温下反应,粉末变红 ( )
(2013·广东理综,23D)
(3)向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含有Fe2+ ( )
(2013·江苏,13D)
(4)Fe3+有氧化性,所以FeCl3溶液可用于回收废旧电路板中的铜 ( )
(2012·广东理综,12D)
(5)在“硫酸亚铁铵的制备”实验中,为了得到硫酸亚铁铵晶体,应小火加热蒸发皿,直到有大量晶体析出时停止加热 ( )
(2012·浙江理综,8C)
(6)过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液,溶液呈血红色,说明稀HNO3将Fe氧化为Fe3+ ( )
(2011·安徽理综,10A)
(7)Fe在足量Cl2中燃烧生成FeCl2和FeCl3 ( )
(2012·天津理综,2D)
(8)Fe分别与氯气和稀盐酸反应所得氯化物相同 ( )
(2011·重庆理综,7A)
(9)Fe与S混合加热生成FeS2 ( )
(2012·重庆理综,7A)
答案 (1)√ (2)× (3)√ (4)√ (5)× (6)× (7)× (8)× (9)×
解析 (2)4H2O(g)+3Fe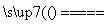 Fe3O4+4H2,粉末变黑。(4)原理为2Fe3++Cu===2Fe2++Cu2+。(5)硫酸亚铁铵是通过降温结晶的方法来制备的,其制备过程是先制成高温饱和溶液,然后冷却,而不是用蒸发结晶的方法来获得的。(6)3Fe+8HNO3(稀)===3Fe(NO3)2+2NO↑+4H2O,所以溶液不呈血红色,因为过量的Fe又把Fe3+还原成Fe2+。(7)Fe在Cl2中燃烧只生成FeCl3。(8)Fe与Cl2反应生成FeCl3,Fe与稀盐酸反应生成FeCl2。(9)Fe与S混合加热生成FeS。
Fe3O4+4H2,粉末变黑。(4)原理为2Fe3++Cu===2Fe2++Cu2+。(5)硫酸亚铁铵是通过降温结晶的方法来制备的,其制备过程是先制成高温饱和溶液,然后冷却,而不是用蒸发结晶的方法来获得的。(6)3Fe+8HNO3(稀)===3Fe(NO3)2+2NO↑+4H2O,所以溶液不呈血红色,因为过量的Fe又把Fe3+还原成Fe2+。(7)Fe在Cl2中燃烧只生成FeCl3。(8)Fe与Cl2反应生成FeCl3,Fe与稀盐酸反应生成FeCl2。(9)Fe与S混合加热生成FeS。


科目:高中化学 来源: 题型:
《茉莉花》是一首脍炙人口的江苏民歌。茉莉花香气的成分有多种,乙酸苯甲酯(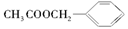
 )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成。一种合成路线如下:
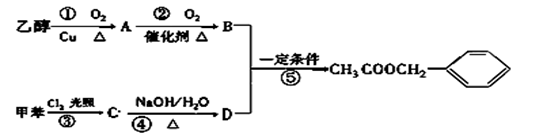
(1)在①②③④⑤五个反应中,属于取代反应的是: (填序号);
(2)B中的含氧官能团的符号是: (写结构式)
(3)D的含苯环的同分异构体中,能使FeCI3溶液显紫色的有 种;
(4)反应⑤ 中120克B与足量的D反应,若B的转化率为60%,则生成乙酸苯甲酯 克
(5)写出乙酸苯甲酯的符合条件的同分异构体的结构简式(写其中一种)
①含苯环,能发生水解反应和银镜反应; ②苯环上有两种不同化学环境的氢原子
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各变化中属于原电池反应的是( )
①在空气中金属铝表面迅速氧化形成保护层,②镀锌铁表面有划损时,仍然能阻止铁被氧化,
③红热的铁丝与冷水接触,表面形成蓝黑色保护层,
④锌与稀硫酸反应时,加入少量CuSO4溶液可使反应加快
A.只有②④ B.只有④ C.只有②③④ D.只有①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
由FeO、Fe2O3和Fe3O4组成的混合物,测得其中铁元素与氧元素的质量比为21∶8,则这种混合物中FeO、Fe2O3和Fe3O4的物质的量之比是 ( )
A.1∶2∶1 B.2∶1∶1
C.1∶3∶1 D.1∶1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:
Ⅰ.向废液中投入过量铁屑,充分反应后分离出固体和滤液;
Ⅱ.向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
(1)FeCl3蚀刻铜箔反应的离子方程式为_____________________________________
________________________________________________________________________。
(2)过程Ⅰ加入铁屑的主要作用是__________________________________________,
分离得到的固体主要成分是____ __________________________________________,
__________________________________________,
从固体中分离出铜需采用的方法是________________________________________。
(3)过程Ⅱ中发生反应的化学方程式为______________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在含有Fe3+、Fe2+、Al3+、NH 的稀溶液中加入足量Na2O2固体,充分反应后,再加入过量稀盐酸,完全反应,则离子数目没有变化的是 ( )
的稀溶液中加入足量Na2O2固体,充分反应后,再加入过量稀盐酸,完全反应,则离子数目没有变化的是 ( )
A.Fe3+、Al3+ B.Al3+
C.Fe2+、NH D.Fe3+
D.Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,若向其中逐渐加入铁粉,溶液中Fe2+浓度和加入铁粉的物质的量之间的关系如下图所示。则稀溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为 (  )
)
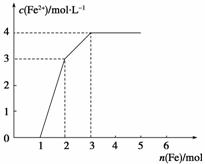
A.1∶1∶1 B.1∶3∶1
C.3∶3∶8 D.1∶1∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,Na2CO3溶液存在水解平衡:CO32-+H2O HCO3-+OH-。下列说法正确的是:
HCO3-+OH-。下列说法正确的是:
A.稀释溶液,水解平衡常数增大 B.通入CO2, 平衡朝正反应方向移动
C.升高温度,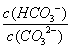 减小 D.加入NaOH固体,溶液pH减小
减小 D.加入NaOH固体,溶液pH减小
查看答案和解析>>
科目:高中化学 来源: 题型:
气体的自动化检测中常常应用原电池原理的传感器。下图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。则下列说法中正确的是

A.上述气体检测时,敏感电极均作电池正极
B.检测Cl2气体时,敏感电极的电极反应为: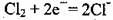
C.检测H2S气体时,对屯极充入空气,对电极上的电极反应式为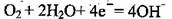
D.检测H2S和体积分数相同的两份空气样本时,传感器上产生的电流大小相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com