
【题目】纯碱和小苏打都是重要的化工原料,在生产和生活中有着广泛的应用。
(1)用洁净的铂丝蘸取Na2CO3溶液置于酒精灯火焰上灼烧,火焰呈__________色。
(2)实验室中需0.2mol/L的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3的质量分别是__________。
A.1000mL;21.2g B.950mL;20.14g C.500mL;21.2g D.500mL;10.6g
(3)若加热10.00g的碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了2.48g,则原混合物中碳酸钠的质量分数为______。
(4)某同学为确定一包可能由碳酸钠和碳酸氢钠组成的白色混合物的成分,他取少量该白色物质溶于水,并向所得溶液中加入适量澄清石灰水,产生白色沉淀,据此该同学认为有碳酸钠。你是否同意该同学的观点,请你用适当的化学方程式阐述你的观点________。
(5)取等物质的量浓度的NaOH溶液两份A和B,每份10 mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如图所示,试回答下列问题:

①曲线A表明,原NaOH溶液中通入CO2后,所得溶液加盐酸后产生CO2气体体积(标准状况)的最大值为_______mL。
②曲线B表明,原NaOH溶液中通入CO2后,所得溶液中的溶质成分是________,其物质的量之比为________。
【答案】黄 A 32.8% 不同意,由于Ca(OH)2 + 2NaHCO3 = CaCO3↓ + Na2CO3 +2H2O (或Ca(OH)2 + NaHCO3 = CaCO3 ↓+ NaOH +H2O),碳酸氢钠溶液与石灰水反应也能产生白色沉淀 33.6 Na2CO3 与 NaHCO3 1:1
【解析】
(1)考查焰色反应;
(2)根据n=cV,m=nM计算;
(3)根据碳酸氢钠加热分解生成碳酸钠,二氧化碳和水,固体质量的减少即为生成二氧化碳的水的质量;
(4)根据碳酸钠,碳酸氢钠与氢氧化钙的反应判断;
(5)①根据碳原子守恒计算二氧化碳的物质的量即为碳酸氢钠的物质的量,利用n=![]() ;②由曲线B可知从25mL到75mL为碳酸氢钠与盐酸反应生成二氧化碳,根据钠原子守恒计算;
;②由曲线B可知从25mL到75mL为碳酸氢钠与盐酸反应生成二氧化碳,根据钠原子守恒计算;
(1)钠的焰色反应为黄色;
(2)配置950ml的溶液应用1000 mL容量瓶配制溶液,所需Na2CO3的质量m=nM=cVM=0.2mol/L×1L×106g/mol=21.2g,答案选A;
(3)设参加反应的碳酸氢钠的质量为x根据混合物质量减少了2.48g,
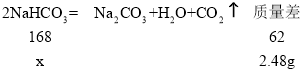
![]() ,解得x=6.72g,碳酸钠和碳酸氢钠共10g,则碳酸钠的质量为10g-6.72g= 3.28g,原混合物中碳酸钠的质量分数=
,解得x=6.72g,碳酸钠和碳酸氢钠共10g,则碳酸钠的质量为10g-6.72g= 3.28g,原混合物中碳酸钠的质量分数=![]() =32.8%;
=32.8%;
(4) 由于Ca(OH)2 + 2NaHCO3 = CaCO3↓ + Na2CO3 +2H2O (或Ca(OH)2 + NaHCO3 = CaCO3 ↓+ NaOH +H2O),碳酸钠与氢氧化钙反应会生成碳酸钙沉淀,同样碳酸氢钠与氢氧化钙反应也会生成碳酸钙沉淀,所以不同意他的观点;
(5) ①CO2与NaOH反应为①CO2+NaOH=NaHCO3,②CO2+2NaOH=Na2CO3+H2O,
当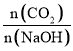 1,反应按①进行,等于1时,CO2、NaOH恰好反应生成NaHCO3;大于1时,生成NaHCO3,CO2有剩余;
1,反应按①进行,等于1时,CO2、NaOH恰好反应生成NaHCO3;大于1时,生成NaHCO3,CO2有剩余;
当![]() <
<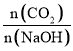 <1,反应按①②进行,CO2、NaOH反应,无剩余,生成物为NaHCO3、Na2CO3;
<1,反应按①②进行,CO2、NaOH反应,无剩余,生成物为NaHCO3、Na2CO3;
当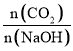
![]() ,反应按②进行,等于
,反应按②进行,等于![]() 时,CO2、NaOH恰好反应生成Na2CO3;小于
时,CO2、NaOH恰好反应生成Na2CO3;小于![]() 时,生成Na2CO3,NaOH有剩余;
时,生成Na2CO3,NaOH有剩余;
由曲线A可知从60ml到75ml为碳酸氢钠与盐酸反应, 消耗的15mL盐酸为碳酸氢钠与盐酸反应并产生CO2,反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,所以n(NaHCO3)=n(HCl)=(75ml60ml)×0.1mol/L=1.5×103mol,根据C原子守恒,所以n(CO2)=n(NaHCO3)=1.5×103mol,V= nVm=1.5×103mol×22.4L/mol=33.6 mL;
② 加入75ml盐酸时二氧化碳的体积达最大,此时溶液为氯化钠溶液。根据氯离子、钠离子守恒,所以n(NaOH)=n(NaCl)=n(HCl)=0.075ml×0.1mol/L=0.0075mol,由曲线B/span>可知从25mL到75mL为碳酸氢钠与盐酸反应生成二氧化碳,反应方程式为NaHCO3+HCl=NaCl+CO2↑+H2O,所以n(NaHCO3)=n(HCl)= n(CO2)=(75ml25ml)×0.1mol/L=0.005mol,所以n(CO2):n(NaOH)=0.005mol:0.0075mol=![]() ,大于1:2,小于1,所以反应按①②进行,CO2、NaOH反应,NaOH无剩余,生成物为Na2CO3 与NaHCO3,根据钠原子守恒,所以
,大于1:2,小于1,所以反应按①②进行,CO2、NaOH反应,NaOH无剩余,生成物为Na2CO3 与NaHCO3,根据钠原子守恒,所以![]() n(Na2CO3)+n(NaHCO3)=0.0075mol,而n(NaHCO3)= 0.005mol,则n(NaHCO3)=0.005mol,故Na2CO3 与NaHCO3的物质的量之比为1:1。
n(Na2CO3)+n(NaHCO3)=0.0075mol,而n(NaHCO3)= 0.005mol,则n(NaHCO3)=0.005mol,故Na2CO3 与NaHCO3的物质的量之比为1:1。


科目:高中化学 来源: 题型:
【题目】Fe与Si形成的合金及铁的配合物用途非常广泛,回答下列问题:
(1)基态Fe2+核外价电子排布式为________;在基态Si原子中,核外存在_____对自旋方向相反的电子。
(2)Fe78Si9B13是一种非晶合金,可通过________方法区分晶体和非晶体。
(3)硅烯是一种具有石墨烯结构的新型二维材料,二硅烯Si2H4分子的几何构型为____,依据电子云的重叠方式可知其所含共价键类型是________。
(4)配合物[Fe(Htrz)3](ClO4) 2 (Htrz为![]() ,1,2,4-三氮唑)
,1,2,4-三氮唑)
①与Fe2+形成配位键的原子是_______;已知分子中的大![]() 键可用
键可用 ![]() 符号表示,其中m代表参与形成大
符号表示,其中m代表参与形成大![]() 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大![]() 键的电子数,则配体
键的电子数,则配体![]() 中的大
中的大![]() 键应表示为_____
键应表示为_____
②1,2,4-三氮唑的沸点为260 ℃,环戊二烯(![]() )的沸点为42.5 ℃,前者的沸点比后者大得多,其原因是_____ 。
)的沸点为42.5 ℃,前者的沸点比后者大得多,其原因是_____ 。
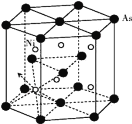
(5)砷化镍晶胞的结构如下图所示,1个砷化镍晶胞中含________个As;若六棱柱底边边长为a cm,高为c cm,阿伏加德罗数的值为NA,则砷化镍的密度为____g/cm3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某空间站中宇航员的呼吸保障系统原理如图所示。

Sabatier系统中发生反应为:
反应I:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)△H1
CH4(g)+2H2O(g)△H1
反应II:CO2(g)+H2(g)![]() CO(g)+H2O(g)△H2=+41.2kJ/mol
CO(g)+H2O(g)△H2=+41.2kJ/mol
(1)常温常压下,已知:
①H2和CH4的燃烧热(△H)分别为-285.5kJ·mol-1和-890.0kJ·mol-1;
②H2O(l)=H2O(g)△H3=+44.0kJ·mol-1。则△H1=__________kJ·mol-1。
(2)按![]() =4的混合气体充入Sabatier系统,当气体总压强为0.1MPa,平衡时各物质的物质的量分数如图所示;不同压强时,CO2的平衡转化率如图所示:
=4的混合气体充入Sabatier系统,当气体总压强为0.1MPa,平衡时各物质的物质的量分数如图所示;不同压强时,CO2的平衡转化率如图所示:

①Sabatier系统中应选择适宜的温度是__________。
②200~550℃时,CO2的物质的量分数随温度升高而增大的原因是__________。
③当温度一定时,随压强升高,CO2的平衡转化率增大,其原因是__________。
(3)一种新的循环利用方案是用Bosch反应[CO2(g)+2H2(g)![]() C(s)+2H2O(g)]代替Sabatier系统。
C(s)+2H2O(g)]代替Sabatier系统。
①分析Bosch反应的熵值变化为:△S__________0(选填“>”或“<”)。
②温度一定时,在2L密闭容器中按![]() =2投料进行Bosch反应,达到平衡时体系的压强为原来压强p0的0.7倍,该温度下反应平衡常数Kp为__________(用含p0的表达式表示,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
=2投料进行Bosch反应,达到平衡时体系的压强为原来压强p0的0.7倍,该温度下反应平衡常数Kp为__________(用含p0的表达式表示,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③下列措施能提高Bosch反应中CO2转化率的是_________(填标号)。
A.加快反应器中气体的流速B.提高原料气中CO2所占比例
C.增大催化剂的表面积D.反应器前段加热,后段冷却
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是( )
A.同温同压下,1 mol N2与1 mol CO可能具有不同的体积
B.同温同压下,二氧化碳与笑气(化学式为N2O)的密度相同
C.质量相同的O2与O3,一定具有相同的原子数
D.28 g CO与1 mol CO一定具有相同的碳原子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠可用于照相业作定影剂、纸浆漂白作脱氯剂等。实验室用SO2通入Na2S和Na2CO3的混合液中来制备硫代硫酸钠。
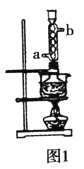
本实验对Na2S纯度要求较高,利用图1所示的装置可将工业级的Na2S提纯。已知Na2S常温下微溶于酒精,加热时溶解度迅速增大,杂质不溶于酒精。提纯过程为:将已称量好的工业级Na2S放入圆底烧瓶中,加入一定质量的酒精和少量水。按图1所示装配所需仪器,向冷凝管通入冷却水,同时水浴加热。待烧瓶中固体不再减少时,停止加热。将烧瓶取下,立即趁热过滤,再冷却结晶,抽滤。将所得固体洗涤、干燥,得到Na2S9H2O晶体。
(1)下列说法不正确的是___。
A.将晶体转移至布氏漏斗时,若器壁上粘有少量晶体,应用冷水淋洗
B.抽滤时,为防止滤纸穿孔,可适当关小水龙头或多加一层滤纸
C.洗涤时,可用一定浓度的乙醇溶液洗涤晶体,目的是洗除晶体表面的杂质,易于得到干燥晶体
D.为加快产品的干燥,可高温烘干
E.在提纯过程中“趁热过滤”操作的目的是防止硫化钠结晶析出而损失、去除杂质
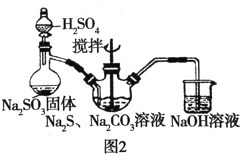
(2)用图2所示装置制取Na2S2O3,其中盛放Na2SO3固体的玻璃仪器名称是________,三颈烧瓶中发生反应的化学方程式__________。
(3)硫代硫酸钠样品中Na2S2O35H2O的纯度(质量分数)可通过氧化还原滴定法测定,相关反应方程式为2Na2S2O3+I2=2NaI+Na2S4O6。准确称取W g样品于锥形瓶中,用适量蒸馏水溶解,并滴加淀粉溶液作指示剂。用0.1000 mol/L碘的标准溶液进行滴定。请回答:
①达到滴定终点的标志是_______。
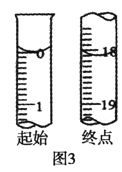
②滴定起始和终点的液面位置如图3,则消耗碘的标准溶液体积为_______ mL,产品纯度为________(设Na2S2O35H2O相对分子质量为M)。
③若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O35H2O的纯度的测量结果________(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氧化二镍(Ni2O3)是一种重要的电子元件材料和蓄电池材料。工业上利用含镍废料(镍、铁、钙、镁合金为主)制取草酸镍(NiC2O4·2H2O),再高温煅烧草酸镍制取Ni2O3.已知草酸的钙、镁、镍盐均难溶于水。工艺流程图如图所示:
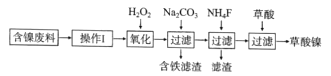
回答下列问题:
(1)“操作I”为“酸浸”,为了提高酸浸的效率,可以采取的措施为__________(写出两条)。
(2)加入H2O2发生的主要反应的离子方程式为________________
(3)加入碳酸钠溶液调pH至4.0~5.0,其目的是___________________
(4)将草酸镍(NiC2O4·2H2O)在热空气中干燥脱水,再采用高温煅烧,可制得Ni2O3,同时获得混合气体,该混合气体的主要成分为水蒸气和_________________
(5)工业上还可用电解法制取Ni2O3用NaOH溶液调 NiCl2,溶液的pH至7.5,加入适量Na 2SO4后利用惰性电极电解。电解过程中产生的Cl2,有80%在弱碱性条件下生成CIO-,再把二价镍氧化为三价镍。CIO-氧化Ni(OH)2生成Ni2O3的离子方程式为_______________________amol二价镍全部转化为三价镍时,外电路中通过电子的物质的量为_______mol.
(6)以Al和NiO(OH)为电极,NaOH溶液为电解液组成原电池,放电时NiO(OH)转化为Ni(OH)2,则放电时负极的电极反应式为_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验中的颜色变化,与氧化还原反应无关的是( )
选项 | 实验操作 | 现象 |
A | AgNO3溶液滴入氯水中 | 产生白色沉淀,随后淡黄绿色逐渐褪去 |
B | FeCl3溶液滴入Mg(OH)2浊液中 | 白色浑浊转化为红褐色沉淀 |
C | H2C2O4溶液滴入KMnO4酸性溶液中 | 产生气泡,随后紫色褪去 |
D | Na块放在坩埚里并加热 | 发出黄色火焰,生成淡黄色固体 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。

(实验一)碘含量的测定。取0.0100mol/L的AgNO3标准溶液装入滴定管,取100.00mL海带浸取原液至滴定池,用电势滴定法测定碘含量。测得的电动势(E)反映溶液中c(I-)的变化,部分数据如下表:
V(AgNO3)/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
E/mV | -225 | -200 | -150 | -100 | 50.0 | 175 | 275 | 300 | 325 |
回答下列问题:
(1)实验中“灼烧”是在__(填仪器名称)中完成的。
(2)用文字具体描述“定容”过程:__
(3)根据表中数据判断滴定终点时用去AgNO3溶液的体积为__mL,计算得海带中碘的质量百分含量为__%。
(实验二)碘的制取。另制海带浸取原液,甲、乙两种实验方案如下:

已知:3I2+6NaOH=5NaI+NaIO3+3H2O。
(4)“适量O2”中能代替O2的最佳物质对应的电子式为__
(5)若要测定“I2+水溶液”中碘的含量,可以选择__作指示剂,用Na2S2O3溶液滴定,滴定终点的现象是__。
(6)若得到“I2+水溶液”时加入硫酸溶液过多,用Na2S2O3溶液滴定时会产生明显的误差,产生此误差的原因为__(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为_____、_____(填标号)。
A. B.
B.
C.![]() D.
D.![]()
(2)Li+与H具有相同的电子构型,r(Li+)小于r(H),原因是______。
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是______、中心原子的杂化形式为______。LiAlH4中,存在_____(填标号)。
A.离子键 B.σ键 C.π键 D.氢键
(4)Li2O是离子晶体,其晶格能可通过图(a)的BornHaber循环计算得到。
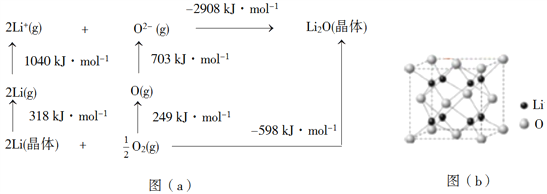
可知,Li原子的第一电离能为________kJ·mol1,O=O键键能为______kJ·mol1,Li2O晶格能为______kJ·mol1。
(5)Li2O具有反萤石结构,晶胞如图(b)所示。已知晶胞参数为0.4665 nm,阿伏加德罗常数的值为NA,则Li2O的密度为______g·cm3(列出计算式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com