
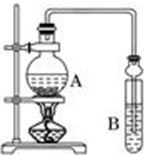
 已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2?6C2H5OH;
已知:①无水氯化钙可与乙醇形成难溶于水的CaCl2?6C2H5OH;| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点(℃) | 34.5 | 78.3 | 118 | 77.1 |
 CH3CO18OC2H5+H2O;
CH3CO18OC2H5+H2O; CH3CO18OC2H5+H2O;
CH3CO18OC2H5+H2O;

 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
| A、增加O2的浓度能加快反应速率 |
| B、降低体系温度能加快反应速率 |
| C、使用催化剂不影响反应速率 |
| D、若反应在密闭容器中进行,2mol SO2和1 mol O2能够生成2mol SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
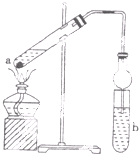 如图,在试管a中先加入2ml.95%的乙醇,加摇边缓缓加入2ml浓硫酸,再加入3ml.无水醋酸,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入7ml.饱和碳酸钠溶液,连接好装置.用酒精灯对试管a加热.当观察到试管b中有明显现象时停止实验.
如图,在试管a中先加入2ml.95%的乙醇,加摇边缓缓加入2ml浓硫酸,再加入3ml.无水醋酸,用玻璃棒充分搅拌后将试管固定在铁架台上,在试管b中加入7ml.饱和碳酸钠溶液,连接好装置.用酒精灯对试管a加热.当观察到试管b中有明显现象时停止实验.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
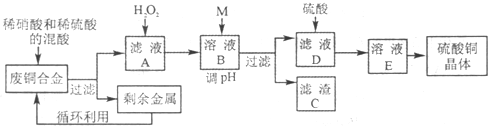
| Fe3+ | Fe2+ | Cu2+ | Al3+ | |
| 开始沉淀时pH | 2.2 | 7.5 | 5.2 | 3.7 |
| 完全沉淀时pH | 3.2 | 9.0 | 6.7 | 4.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 漂粉精加盐酸所释放出的氯气 |
| 漂粉精的质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 步骤 | 检验离 子 | 检验方法 | 现象 | 离子方程式 |
| Ⅰ | ① | 焰色反应 | 火焰呈紫色(透过蓝色钴玻璃) | |
| Ⅱ | Al3+ | 将氢氧化钠溶液逐滴加入到明矾溶液止过量 | ②先观察到: | Al3++3OH-=Al(OH)3↓ |
| 后观察到: | ③ | |||
| Ⅲ | SO42- | ④先加 | 无明显现象 | |
| 后加 | 产生白色沉淀 | Ba2++SO42-=BaSO4↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com