
下列几种金属的冶炼中,属于分解反应的有
[ ]
 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:
| 元素 | 钠 | 镁 | 铝 | 硅 |
| 电负性 | 0.9 | 1.2 | x | 1.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
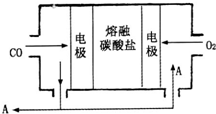 (2013?德州模拟)钠及其化合物具有广泛的用途.
(2013?德州模拟)钠及其化合物具有广泛的用途.
| ||
| ||
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属被利用的早晚取决于其在地壳中的含量,在地壳中含量越高,被利用的越早 | B、金属冶炼的实质是金属阳离子借助于还原反应转化为金属单质的过程 | C、工业上冶炼铝是利用C或者CO还原Al2O3得到单质铝 | D、工业上冶炼铁利用还原剂CO通过置换反应得到单质铁 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年北京市西城区高三第二次模拟考试理综化学试卷(解析版) 题型:填空题
铝及其化合物在生产生活中具有重要的作用。
(1)铝在元素周期表中的位置是 。
(2)已知电负性的数值表示原子对电子吸引能力的相对大小。以下是几种原子的电负性数值:
|
元素 |
钠 |
镁 |
铝 |
硅 |
|
电负性 |
0.9 |
1.2 |
χ |
1.8 |
①铝的电负性χ的范围是 。
②电负性的数值与元素金属性的关系是 。
③下列实验能比较镁和铝的金属性强弱的是 。
a.测定镁和铝的导电性强弱
b.测定等物质的量浓度的Al2(SO4)3和MgSO4溶液的pH
c.向0.1 mol/LAlCl3和0.1 mol/L MgCl2中加过量NaOH溶液
(3)铝热法是常用的金属冶炼方法之一。
已知:4Al(s)+3O2(g)=2Al2O3(s) ΔH1=-3352 kJ/mol
Mn(s)+O2(g)=MnO2(s) ΔH2= -521 kJ/mol
Al与MnO2反应冶炼金属Mn的热化学方程式是 。
(4)冶炼金属铝时,用石墨做电极电解熔融Al2O3。液态铝在(填“阴”或“阳”) 极得到,电解过程中,阳极石墨需要不断补充,结合电极反应说明其原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com