
分析 (1)整个过程最终生成为Na2SO4,根据钠离子守恒可知:2n(Na2SO4)=2n(Na2CO3)+n(NaOH),据此计算n(Na2CO3),再根据碳元素守恒计算n(CO2),根据V=nVm计算CO2的体积;
(2)根据m=nM计算Na2CO3的质量,进而计算样品中无水碳酸钠的纯度.
解答 解:(1)整个过程最终生成为Na2SO4,根据钠离子守恒可知:2n(Na2SO4)=2n(Na2CO3)+n(NaOH),则:
2×0.05L×0.1mol/L=2n(Na2CO3)+0.04L×0.1mol/L,
解得n(Na2CO3)=0.003mol,
根据碳元素守恒,可知n(CO2)=n(Na2CO3)=0.003mol,故V(CO2)=0.003L×22.4L/mol=0.0672L=67.2mL,
答:标况下生成二氧化碳的体积为67.2mL;
(2)Na2CO3的质量=0.003mol×106g/mol=0.318g,故样品中无水碳酸钠的纯度=$\frac{0.318g}{0.4g}$×100%=79.5%,
答:样品中无水碳酸钠的纯度为79.5%.
点评 本题考查化学方程式的有关计算,明确发生的反应是解题关键,本题利用守恒思想解答,避免利用方程式计算的繁琐,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 胶粒可以导电 | B. | 胶体是混合物 | ||
| C. | 胶体的分散剂为气体 | D. | 胶体粒子大小在1~100nm 之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 操作和现象 | 结论 | |
| A | 切开金属钠,钠表面银白色会逐渐褪去 | Na在空气中会生成Na2O2 |
| B | 铁棒插入浓硝酸中,无明显现象 | 铁与浓硝酸不反应 |
| C | 将FeCl2溶液滴加到少许酸性KMnO4溶液中,溶液褪色 | FeCl2具有漂白性 |
| D | 向Fe(NO3)2溶液中滴加稀硫酸和KSCN溶液,溶液变成红色 | 原溶液中可能含有Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
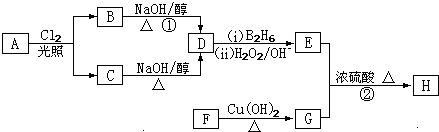
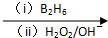 R-CH2CH2OH(B2 H6为乙硼烷)
R-CH2CH2OH(B2 H6为乙硼烷) ;
; ;
;查看答案和解析>>
科目:高中化学 来源: 题型:推断题
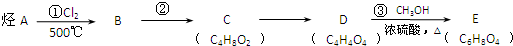
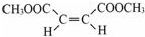 .
.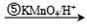 $\stackrel{⑥}{→}$$\stackrel{⑦酸化}{→}$D.则⑥所需的无机试剂及反应条件是NaOH的醇溶液、加热;④的化学方程式是
$\stackrel{⑥}{→}$$\stackrel{⑦酸化}{→}$D.则⑥所需的无机试剂及反应条件是NaOH的醇溶液、加热;④的化学方程式是 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤 | 预期现象和结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
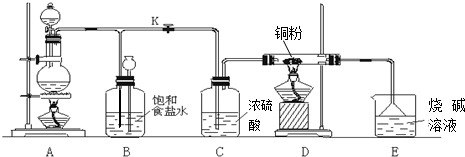
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 待提纯样品(括号内为杂质) | 除杂方法或实验装置 |
| A | 淀粉胶体(KI溶液) | 过滤 |
| B | 乙酸乙酯(饱和碳酸钠溶液) | 蒸馏,收集77℃下馏分 |
| C | CO2(SO2) | 通过盛有饱和碳酸钠溶液的洗气瓶并干燥 |
| D | 氯气(氯化氢) | 通过盛有饱和食盐水的洗气瓶并干燥 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com