
可逆反应:3A(g) 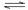 3B(?)+C(?);ΔH>0,随着温度的升高,气体平均相对分子质量有变小的趋势,则下列判断正确的是 ( )
3B(?)+C(?);ΔH>0,随着温度的升高,气体平均相对分子质量有变小的趋势,则下列判断正确的是 ( )
A.B和C可能都是固体 B. 若C为固体,则B一定是气体
C. B和C一定都是气体 D. B和C不可能都是气体
 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:
下列对高分子材料的研究方向,不正确的一项是( )
A.使高分子材料具有仿生能力
B.使高分子材料向功能材料方向发展
C.使高分子材料越来越牢固,难分解
D.使农用薄膜能够选择性地透过某种植物所需要的特定波长的光
查看答案和解析>>
科目:高中化学 来源: 题型:
CuSO4在活化闪锌矿(主要成分是ZnS)方面有重要作用,主要是活化过程中生成CuS、Cu2S等一系列铜的硫化物活化组分。
(1)Cu2+基态的电子排布式可表示为 ;
(2)SO42-的空间构型为 (用文字描述);中心原子采用的轨道杂化方式是 ;写出一种与SO42-互为等电子体的分子的化学式: ;
(3) 向CuSO4 溶液中加入过量NaOH溶液可生成[Cu (OH)4 ]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为 ;
(4)资料显示ZnS为难溶物,在活化过程中,CuSO4能转化为CuS的原因是 。
(5)CuS比CuO的熔点 (填高或低),原因是 。
(6)闪锌矿的主要成分ZnS,晶体结构如下图所示,其晶胞边长为540.0 pm,密度为____________(列式并计算),a位置S2-离子与b位置Zn2+离子之间的距离为___________________pm(列式表示)。
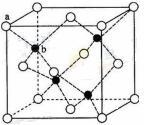
查看答案和解析>>
科目:高中化学 来源: 题型:
①1 mol某链烃最多能和2 mol HCl发生加成反应,生成1 mol氯代烷;②1 mol该氯代烷能和8 mol Cl2发生取代反应,生成只含碳元素和氯元素的氯代烃。该链烃可能是 ( )。
A.CH3CH===CH2  B.CH2===CHCH===CH2
B.CH2===CHCH===CH2
C.CH3CH===CHCH3 D.CH3C≡CH
查看答案和解析>>
科目:高中化学 来源: 题型:
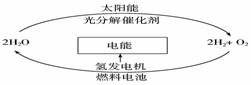 科学家预测“氢能”将是人类社会最理想的新能源,目前,有人提出一种最经济最理想的获得氢能源的循环体系,如下图所示。下列说法错误的是 ( )
科学家预测“氢能”将是人类社会最理想的新能源,目前,有人提出一种最经济最理想的获得氢能源的循环体系,如下图所示。下列说法错误的是 ( )
A.在氢能的利用过程中,H2O可循环使用
B.氢气、氧气和稀硫酸构成的燃料电池中,正极的电极反应为:O2 + 4e- + 2H2O = 4OH-
C.该法制氢的关键是寻找光分解催化剂
D.利用光电转化可将太阳能转化为电能用于电解水而获得氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
已知3.6g碳在6.4g的氧气中燃烧,至反应物耗尽,并放出X kJ热量。已知单质碳的燃烧
热为-Y kJ/mol,则C与1mol O2反应生成CO时的反应热△H为 ( )
A-Y kJ/mol B-(10X-Y)kJ/mol C-(5X-0.5Y)kJ/mol D+(10X-Y)kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
在400℃,1.01X105Pa时,将SO2和14molO2 压入一个装有催化剂的VL密闭反应器中,发生2SO2+O2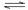 2SO3的反应,并且在10min后达到平衡时,测得容器内有2molSO2和12molO2
2SO3的反应,并且在10min后达到平衡时,测得容器内有2molSO2和12molO2
(1)SO2的起始浓度为_________,SO3(g)的平衡浓度为_________;
(2)SO2的转化率为_________,O2的平均反应速率为_________;
(3)平衡时SO3占总体积的百分数为________________,
此时体系压强为反应起始时体系压强的________倍;
(4)达平衡后再加入2molSO2、12molO2和4molSO3(g),此时正反应速率将__________,
逆反应速率将__________(填“增大”,“减小”或“不变”),平衡__________移动(填“向左”,“向右”或“不”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知An+、B(n-1)+、C(n+1)+、D(n+1)-都有相同的电子层结构,A、B、C、D的原子半径由大到小的顺序是( )
A.B>A>C>D B.A>B>C>D C.C>D>B>A D.A>B>D>C
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B和C三种主族元素,若A元素的阴离子与B、C元素的阳离子具有相同的电子层结构,且B的阳离子半径大于C的阳离子半径,则这三种元素的原子序数大小次序是( )
A.B<C<A B.A<B<C
C.C<B<A D.B>C>A
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com