
”¾ĢāÄæ”æŌŚÄ³NaClČÜŅŗѳʷ֊ŗ¬ÓŠNa2SO4”¢CaCl2ŌÓÖŹ(øĆČÜŅŗÓĆX±ķŹ¾)”£³żČ„ŌÓÖŹµÄŹµŃé·½°øČēĻĀ£ŗ

(1)BČÜŅŗÖŠ“ęŌŚµÄŃōĄė×ÓÓŠ_________£¬ŅõĄė×ÓÓŠ_________”£
(2)CÖŠĖłŗ¬ĪļÖŹµÄ»ÆѧŹ½ŹĒ_________”£
(3)DÖŠ¼ÓČėŹŹĮæŃĪĖįŗ󣬓óĮæ¼õÉŁµÄĪ¢Į£ÓŠ__________”£
(4)¢ŁŗĶ¢Ś²»Äܵ÷»»Ė³ŠņµÄĄķÓÉŹĒ__________”£
(5)ijĶ¬Ń§ČĻĪŖæɽ«ÉĻ·½°ø½ųŠŠøĽų£ŗ¢Ł¼ÓČė¹żĮæBaCO3 ¢Ś¼ÓČėŹŹĮæŃĪĖį£¬¼“æÉ“ļµ½³żŌÓµÄÄæµÄ£¬¶ųĒŅ²½ÖčøüĪŖ¼ņ±ć”£ĒėĘĄ¼ŪÕāÖÖ·½·ØŹĒ·ńÕżČ·______£¬ĖµĆ÷ĄķÓÉ_________”£
”¾“š°ø”æNa£«”¢Ba2+”¢Ca2+ Cl- CaCO3 BaCO3 CO32- ¢ŁŗĶ¢Śµ÷»»Ė³ŠņĖäČ»Ņ²æÉŅŌ³żČ„Ca2+ ŗĶSO42-£¬µ«ŹĒŗó¼ÓČėµÄBaCl2ČÜŅŗÖŠµÄBa2+ŅŌŌÓÖŹµÄŠĪŹ½ĮōŌŚČÜŅŗÖŠ£¬Ī“³żČ„ ²»ÕżČ· ŅņĪŖBaCO3ÄŃČÜÓŚĖ®£¬ÓėNa2SO4”¢CaCl2ÄŃŅŌ·¢Éś·“Ó¦£¬ĪŽ·Øµ½“ļ³żČ„ŌÓÖŹµÄÄæµÄ
”¾½āĪö”æ
ijNaClČÜŅŗѳʷ֊ŗ¬ÓŠNa2SO4”¢CaCl2ŌÓÖŹ£¬¼ÓČėBaCl2ŗóÉś³ÉBaSO4°×É«³Į¶Ø£¬¹żĀĖŗóĀĖŅŗBÖŠŗ¬ÓŠNaCl ”¢CaCl2 ”¢BaCl2³É·Ö£¬ŌŁ¼ÓČė¹żĮæµÄNa2CO3Éś³É³ĮµķCĪŖBaCO3£¬CaCO3£¬¹żĀĖŗóĀĖŅŗDŗ¬ÓŠNaCl ”¢Na2CO3£¬ŌŁ¼ÓŹŹĮæµÄHClČÜŅŗ£¬ČÜŅŗ±äĪŖNaCl”£
(1)×ŪŗĻÉĻŹö·ÖĪöÖŖ: BÖŠŗ¬ÓŠNaCl ”¢CaCl2 ”¢BaCl2³É·Ö£¬ĖłŅŌBČÜŅŗÖŠ“ęŌŚµÄŃōĄė×ÓÓŠNa£«”¢Ba2+”¢Ca2+£¬ŅõĄė×ÓÓŠCl-”£“š°ø£ŗNa£«”¢Ba2+”¢Ca2+ £»Cl-”£
(2) ×ŪŗĻÉĻŹö·ÖĪöÖŖ: ¼ÓČė¹żĮæµÄNa2CO3Éś³É³ĮµķCĪŖBaCO3£¬CaCO3£¬ĖłŅŌCÖŠŗ¬ÓŠŗ¬ÓŠµÄĪļÖŹµÄ»ÆѧŹ½ŹĒ£ŗCaCO3 ”¢BaCO3”£“š°ø£ŗCaCO3 ”¢BaCO3”£
(3) ×ŪŗĻÉĻŹö·ÖĪöÖŖDŗ¬ÓŠNaCl ”¢Na2CO3£¬¼ÓČėŹŹĮæŃĪĖįŗó£¬2H++ CO32-=H2O+CO2![]() ,“óĮæ¼õÉŁµÄĪ¢Į£ŹĒCO32-”£“š°ø£ŗCO32-”£
,“óĮæ¼õÉŁµÄĪ¢Į£ŹĒCO32-”£“š°ø£ŗCO32-”£
(4) ¢ŁŗĶ¢Śµ÷»»Ė³ŠņĖäČ»Ņ²æÉŅŌ³żČ„Ca2+ ŗĶSO42-£¬µ«ŹĒŗó¼ÓČėµÄBaCl2ČÜŅŗÖŠµÄBa2+ŅŌŌÓÖŹµÄŠĪŹ½ĮōŌŚČÜŅŗÖŠ£¬²»ÄܳżČ„£¬¹Ź¢ŁŗĶ¢Ś²»Äܵ÷»»”£“š°ø: ¢ŁŗĶ¢Śµ÷»»Ė³ŠņĖäČ»Ņ²æÉŅŌ³żČ„Ca2+ ŗĶSO42-£¬µ«ŹĒŗó¼ÓČėµÄBaCl2ČÜŅŗÖŠµÄBa2+ŅŌŌÓÖŹµÄŠĪŹ½ĮōŌŚČÜŅŗÖŠ£¬Ī“³żČ„”£
(5)øĆĶ¬Ń§µÄøĽų·½·Ø²»ŗĻĄķ£¬ŅņĪŖBaCO3ÄŃČÜÓŚĖ®£¬ÓėNa2SO4”¢CaCl2ÄŃŅŌ·¢Éś·“Ó¦£¬ĪŽ·Øµ½“ļ³żČ„ŌÓÖŹµÄÄæµÄ£¬“š°ø£ŗ²»ÕżČ·£»ŅņĪŖBaCO3ÄŃČÜÓŚĖ®£¬ÓėNa2SO4”¢CaCl2ÄŃŅŌ·¢Éś·“Ó¦£¬ĪŽ·Øµ½“ļ³żČ„ŌÓÖŹµÄÄæµÄ”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¹żĢ¼ĖįÄĘ(Na2CO3”¤3H2O2) ŌŚĻ“µÓ”¢·ÄÖÆ”¢Ņ½Ņ©µČĮģÓņÓŠ¹ć·ŗÓ¦ÓĆ”£Ņ»ÖÖÖʱø¹żĢ¼ĖįÄĘµÄ¹¤ŅÕĮ÷³ĢČēĶ¼ĖłŹ¾”£

£Ø1£©Ģ¼ĖįÄĘĖ®ČÜŅŗ³Ź¼īŠŌµÄŌŅņŹĒ____________(ÓĆĄė×Ó·½³ĢŹ½±ķŹ¾)£¬ĪŖŌöĒæĻ“µÓŠ§¹ū£¬æɲÉČ”×ī¼ņµ„µÄ“ėŹ©ŹĒ________________”£
£Ø2£©¹żĢ¼ĖįÄĘŹÜČČŅ×·Ö½ā£¬Š“³ö·“Ó¦µÄ»Æѧ·½³ĢŹ½:__________________
£Ø3£©ĪČ¶Ø¼ĮæÉÄÜŹĒ_____(ĢīŠņŗÅ)”£
A.Na2SO3 B.Na2SiO3 C.H2SO4 D.MnO2
£Ø4£©½į¾§Ź±¼ÓČėŹ³ŃĪµÄÄæµÄŹĒ_________,ÄøŅŗÖŠæÉŃ»·Ź¹ÓƵÄĪļÖŹŹĒ_________(Ģī»ÆѧŹ½)”£
£Ø5£©¹¤ŅµÉĻ³£ŅŌ¹żĢ¼ĖįÄĘ²śĘ·ÖŠ»īŠŌŗ¬ŃõĮæ![]() Ą“ŗāĮæ²śĘ·ÓÅĮÓ£¬13%ŅŌÉĻµÄĪŖÓÅÖŹĘ·”£²śĘ·ÖŠ»īŠŌŃõŗ¬ĮæµÄ²ā¶Ø·½·Ø: ³ĘĮæm g ѳʷ£¬ŌŚ250mL ׶ŠĪĘæÖŠÓĆ100mL 0.5mol/LĮņĖįĶźČ«Čܽā£¬Į¢¼“ÓĆc mol/LµÄøßĆĢĖį¼Ų±ź×¼ČÜŅŗ½ųŠŠµĪ¶Ø£¬ÖĮµĪ¶ØÖÕµć£¬¹ż³ĢÖŠMnO2±»»¹ŌĪŖMn2+,½ųŠŠČż“ĪµĪ¶Ø£¬²āµĆĻūŗıź×¼ČÜŅŗĘ½¾łĢå»żĪŖV1mL”£ĮķĶā£¬ŌŚ²»¼ÓѳʷµÄĒéæöĻĀ°“ÕÕÉĻŹö¹ż³Ģ½ųŠŠæÕ°×ŹµŃ飬ĻūŗÄøßĆĢĖį¼ŲČÜŅŗµÄĢå»żĪŖV2 mL”£øĆ²śĘ·»īŠŌŃõŗ¬ĮæĪŖ________(ÓĆ“śŹżŹ½±ķŹ¾)”£
Ą“ŗāĮæ²śĘ·ÓÅĮÓ£¬13%ŅŌÉĻµÄĪŖÓÅÖŹĘ·”£²śĘ·ÖŠ»īŠŌŃõŗ¬ĮæµÄ²ā¶Ø·½·Ø: ³ĘĮæm g ѳʷ£¬ŌŚ250mL ׶ŠĪĘæÖŠÓĆ100mL 0.5mol/LĮņĖįĶźČ«Čܽā£¬Į¢¼“ÓĆc mol/LµÄøßĆĢĖį¼Ų±ź×¼ČÜŅŗ½ųŠŠµĪ¶Ø£¬ÖĮµĪ¶ØÖÕµć£¬¹ż³ĢÖŠMnO2±»»¹ŌĪŖMn2+,½ųŠŠČż“ĪµĪ¶Ø£¬²āµĆĻūŗıź×¼ČÜŅŗĘ½¾łĢå»żĪŖV1mL”£ĮķĶā£¬ŌŚ²»¼ÓѳʷµÄĒéæöĻĀ°“ÕÕÉĻŹö¹ż³Ģ½ųŠŠæÕ°×ŹµŃ飬ĻūŗÄøßĆĢĖį¼ŲČÜŅŗµÄĢå»żĪŖV2 mL”£øĆ²śĘ·»īŠŌŃõŗ¬ĮæĪŖ________(ÓĆ“śŹżŹ½±ķŹ¾)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©³£ĪĀŹ±£¬½«ÅضČĪŖm molL©1µÄCH3COOHČÜŅŗŗĶn molL©1 NaOHČÜŅŗµČĢå»ż»ģŗĻ£¬»ģŗĻŗóČÜŅŗµÄpH=7£¬mÓėnµÄ“󊔹ŲĻµŹĒm____ n£ØĢī”°£¾”±”¢”°£¼”±»ņ”°=”±£¬ĻĀĶ¬£©£»Čō½«pH=2µÄCH3COOHČÜŅŗŗĶpH=12µÄNaOHČÜŅŗµČĢå»ż»ģŗĻ£¬»ģŗĻČÜŅŗµÄpH______ 7”£
£Ø2£©Ļū·ĄÓƵÄÅŻÄĆš»šĘ÷ČװµÄŅ©Ę·ŹĒĮņĖįĀĮČÜŅŗŗĶĢ¼ĖįĒāÄĘČÜŅŗ£¬ÓĆĄė×Ó·½³ĢŹ½±ķŹ¾¶žÕß»ģŗĻŹ±·¢ÉśµÄ·“Ó¦_________________.
£Ø3£©³£ĪĀĻĀijĒæĖįČÜŅŗpH=a£¬Ēæ¼īČÜŅŗpH=b£¬ŅŃÖŖa+b=12£¬Ėį¼īČÜŅŗ»ģŗĻpH=7£¬ŌņĖįČÜŅŗĢå»żV1ŗĶ¼īČÜŅŗĢå»żV2µÄ¹ŲĻµĪŖ_________.
£Ø4£©³£ĪĀŹ±Ksp[Cu(OH)2]=2.2”Į10©20£¬½«Cu(OH)2ČÜÓŚ2.2mol/L CuCl2ČÜŅŗÖŠŠĪ³ÉĘ½ŗāČÜŅŗµÄpHĪŖ____.
£Ø5£©ĪļÖŹµÄĮæÅضČĻąĶ¬µÄĻĀĮŠČÜŅŗ¢Ł(NH4)2CO3¢Ś(NH4)2SO4¢ŪNH4HCO3¢ÜNH4HSO4¢ŻNH4Cl¢ŽNH3H2O£¬c£ØNH4+£©ÓÉŠ”µ½“óµÄÅÅĮŠĖ³ŠņŹĒ___________£ØĢīŠņŗÅ£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÖŠ£¬²»ÕżČ·µÄŹĒ
A. 0.1 mol N2µÄÖŹĮæŹĒ2.8 g
B. MgµÄĦ¶ūÖŹĮæŹĒ24 g/mol
C. 2 L 0.1mol”¤L£1NaClČÜŅŗÖŠ£¬c(Na£«)£½0.2mol”¤L£1
D. ±ź×¼×“æöĻĀ£¬11.2 L O2ŗ¬ÓŠµÄŌ×ÓŹżÄæŌ¼ĪŖ6.02”Į1023
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”湤ŅµÉĻÓĆĻ“¾»µÄ·ĻĶŠ¼×öŌĮĻĄ“ÖʱøĻõĖįĶ£¬“Ó½ŚŌ¼ŌĄķ¼°·ĄÖĪĪŪČ¾»·¾³µÄ½Ē¶Čæ¼ĀĒ£¬ŅĖ²ÉČ”µÄ·½·ØŹĒ
A. Cu+HNO3(ÅØ)”śCu(NO3) 2
B. Cu+HNO3(Ļ”)”śCu(NO3) 2
C. Cu ![]() CuO
CuO ![]() Cu(NO3)2
Cu(NO3)2
D. Cu ![]() CuSO4
CuSO4 ![]() Cu(NO3)2
Cu(NO3)2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĢõ¼žĻĀ£¬ĶعżĻĀĮŠ·“Ó¦æÉŹµĻÖČ¼ĆŗŃĢĘųÖŠĮņµÄ»ŲŹÕ£ŗ
SO2(g)+2CO(g)![]() 2CO2(g)+S(l)”÷H£¼0 Čō·“Ó¦ŌŚŗćČŻµÄĆܱÕČŻĘ÷ÖŠ½ųŠŠ£¬ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
2CO2(g)+S(l)”÷H£¼0 Čō·“Ó¦ŌŚŗćČŻµÄĆܱÕČŻĘ÷ÖŠ½ųŠŠ£¬ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
A. Ę½ŗāĒ°£¬Ėę×Å·“Ó¦µÄ½ųŠŠ£¬ČŻĘ÷ÄŚŃ¹ĒæŹ¼ÖÕ²»±ä
B. Ę½ŗāŹ±£¬ĘäĖūĢõ¼ž²»±ä£¬·ÖĄė³öĮņ£¬Õż·“Ó¦ĖŁĀŹ¼Óæģ
C. Ę½ŗāŹ±£¬ĘäĖūĢõ¼ž²»±ä£¬ÉżøßĪĀ¶ČæÉĢįøßSO2µÄ×Ŗ»ÆĀŹ
D. ĘäĖūĢõ¼ž²»±ä£¬Ź¹ÓĆ²»Ķ¬“߻ƼĮ£¬øĆ·“Ó¦Ę½ŗā³£Źż²»±ä
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŃŠ¾æµŖµÄŃ»·ŗĶ×Ŗ»Æ¶ŌÉś²ś”¢Éś»īÓŠÖŲŅŖµÄ¼ŪÖµ”£
I£®(1)Š“³öŹµŃéŹŅÖʱø°±ĘųµÄ»Æѧ·½³ĢŹ½________ ”£
II£®°±ŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ”£Ä³¹¤³§ÓĆ°±ÖĘĻõĖįŗĶļ§ŃĪµÄĮ÷³ĢČēĻĀĶ¼ĖłŹ¾”£

(2)Éč±ø1”¢3ÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½·Ö±šŹĒ______”¢ ________ ”£Éč±ø2ÖŠĶØČėµÄĪļÖŹAŹĒ________”£
III£®°±µŖ·ĻĖ®µÄČ„³żŹĒµ±Ē°æĘѧъ¾æµÄČȵćĪŹĢā”£°±µŖ·ĻĖ®ÖŠµÄµŖŌŖĖŲ¶ąŅŌNH4+ŗĶNH3H2OµÄŠĪŹ½“ęŌŚ”£Ä³¹¤³§“¦Ąķ°±µŖ·ĻĖ®µÄĮ÷³ĢČēĻĀ£ŗ

(3)¹ż³Ģ¢ŁµÄÄæµÄŹĒ½«NH4+×Ŗ»ÆĪŖNH3£¬²¢Ķعż¹ÄČė“óĮææÕĘų½«°±Ęų“µ³ö£¬Š“³öNH4+×Ŗ»ÆĪŖNH3µÄĄė×Ó·½³ĢŹ½________ ”£
(4)¹ż³Ģ¢Ś¼ÓČėNaClOČÜŅŗæɽ«°±µŖ×Ŗ»ÆĪŖĪŽ¶¾ĪļÖŹ£¬·“Ó¦ŗóŗ¬µŖŌŖĖŲ”¢ĀČŌŖĖŲµÄĪļÖŹ»ÆѧŹ½·Ö±šĪŖ___”¢_______”£
(5)ŗ¬ÓąĀČ·ĻĖ®µÄÖ÷ŅŖ³É·ÖŹĒNaClOŅŌ¼°HClO£¬XæÉŃ”ÓĆŅŌĻĀÄÄÖÖČÜŅŗŅŌ“ļµ½Č„³żÓąĀȵÄÄæµÄ(ĢīŠņŗÅ)_________”£
a£®KOH b£®Na2SO3 c£®KMnO4 D£®NaCl
Š“³öĘäÖŠŅ»øö·“Ó¦µÄĄė×Ó·½³ĢŹ½__________ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ©Īļ±“ŵõ„æÉÓÉŅŅõ£Ė®ŃīĖįŗĶ¶ŌŅŅõ£°±»ł·ÓŌŚŅ»¶ØĢõ¼žĻĀ·“Ó¦ÖĘµĆ£ŗ
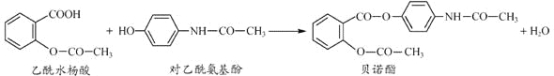
ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ£Ø £©
A. ±“ŵõ„·Ö×ÓÖŠÓŠČżÖÖŗ¬Ńõ¹ŁÄÜĶÅ
B. æÉÓĆFeCl3ČÜŅŗĒų±šŅŅõ£Ė®ŃīĖįŗĶ¶ŌŅŅõ£°±»ł·Ó
C. ŅŅõ£Ė®ŃīĖįŗĶ¶ŌŅŅõ£°±»ł·Ó¾łÄÜÓėNaHCO3ČÜŅŗ·“Ó¦
D. ±“ŵõ„Óė×ćĮæNaOH ČÜŅŗ¹²ČČ£¬×īÖÕÉś³ÉŅŅõ£Ė®ŃīĖįÄĘŗĶ¶ŌŅŅõ£°±»ł·ÓÄĘ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠ»śĪļµÄ½į¹¹æÉÓĆ¼üĻߏ½¼ņ»Æ±ķŹ¾£¬ČēCH3-CH=CH-CH3æɱķŹ¾ĪŖ![]() £¬ÓŠŅ»ÖÖÓŠ»śĪļXµÄ¼üĻߏ½ČēĶ¼ĖłŹ¾”£
£¬ÓŠŅ»ÖÖÓŠ»śĪļXµÄ¼üĻߏ½ČēĶ¼ĖłŹ¾”£

(1)XµÄ·Ö×ÓŹ½ĪŖ_______________________”£
(2)ÓŠ»śĪļYŹĒXµÄĶ¬·ÖŅģ¹¹Ģ壬ĒŅŹōÓŚ·¼Ļć×å»ÆŗĻĪļ”£ŌņYµÄ½į¹¹¼ņŹ½ŹĒ_____________”£
(3)YŌŚŅ»¶ØĢõ¼žĻĀæÉ·¢Éś·“Ӧɜ³Éøß·Ö×Ó»ÆŗĻĪļ£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ_________________”£
(4)YæÉŅŌÓėäåĖ®·“Ó¦£¬øĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ____________________________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com