
���� ���ݸ��ݸ�˹��������������ѧƽ�ⳣ������ƽ��״̬��������ƽ��Ũ�ȵ��ݴη��˻����Է�Ӧ����ݴη��˻������ݻ�ѧƽ�ⳣ����Ӱ���������жϣ�
��� �⣺��2N2��g��+6H2O��1��?4NH3��g��+3O2��g����H=+1530kJ/mol
��H2O��1��=H2O��g����H=+44.0kJ/mol
�ɢ�-�ڡ�6�ã�2N2��g��+6H2O��g��?4NH3��g��+3O2��g����H=+1266kJ/mol��
�÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK=$\frac{{C}^{4}��N{H}_{3}��{C}^{3}��{O}_{2}��}{{C}^{2}��{N}_{2}��{C}^{6}��{H}_{2}O��}$��
��ѧƽ�ⳣ���Ĵ�Сֻ���¶��йأ�������ѹǿ��Kֵ���䣬
�ʴ�Ϊ��+1266��$\frac{{C}^{4}��N{H}_{3}��{C}^{3}��{O}_{2}��}{{C}^{2}��{N}_{2}��{C}^{6}��{H}_{2}O��}$�����䣮
���� ���⿼���˹���ɵ�Ӧ�á���ѧƽ�ⳣ�����Ѷ��еȣ��ؼ�ץס����Ӧ����֪��Ӧ����ʽ֮��Ĺ�ϵ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2ͨ�����ʯ��ˮ�� | B�� | Na2CO3��Һ�е���HCl��Һ | ||
| C�� | �����м���п�� | D�� | ��˿��������ȼ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ұ�����İ�ɫ�̳� | B�� | ʯ��Ҥ�İ�ɫ�۳� | ||
| C�� | ��ɫ�������� | D�� | ����ϩ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
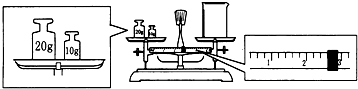
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��4 | B�� | 1��5 | C�� | 2��1 | D�� | 2��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | Cl2+2KBr�TBr2+2KCl | B�� | 2NaHCO3�TNa2CO3+H2O+CO2�� | ||
| C�� | 4Fe��OH��2+O2+2H2O�T4Fe��OH��3 | D�� | 2K2O2+2CO2�T2K2CO3+O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���˷� | B�� | ���� | C�� | ��Һ�� | D�� | ��ȡ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com