
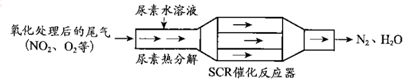
分析 (1)①尿素[CO(NH2)2]水溶液热分解为NH3和CO2,结合原子守恒配平书写化学方程式;
②反应器中NH3还原NO2生成氮气和水,根据电子守恒和原子守恒可得此反应的化学方程式;
③SO2在O2作用下与NH3、H2O反应形成(NH4)2SO4,此反应中SO2是还原剂,氧气是氧化剂,结合电子守恒和原子守恒可得此反应的化学方程式;
④涉及反应为2NH3+H2SO4=n(NH4)2SO4,2NaOH+H2SO4=Na2SO4+H2O,由方程式可知n(NaOH)+n(NH3)=2n(H2SO4),以此计算;
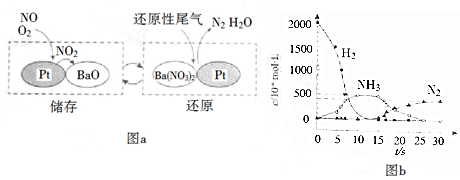
(2)①由图a可知储存NOx的物质是BaO;
②第一步反应中H2被氧化生成水,化合价由0价升高到+1价,Ba(NO3)2的N元素化合价由+5价降低到-3价,生成氨气,结合得失电子数目相等计算;
③在有氧条件下15NO与NH3以一定比例反应时,得到的笑气几乎都是15NNO,由N元素守恒可知15NO与NH3应为1:1,结合电子得失相等配平.
解答 解:(1)①尿素[CO(NH2)2]水溶液热分解为NH3和CO2,反应物为尿素和水,反应生成物为氨气和水,原子守恒书写化学方程式为:CO(NH2)2+H2O$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CO2↑,
故答案为:CO(NH2)2+H2O$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CO2↑;
②NH3在催化剂作用下还原NO2生成氮气和水,反应的化学方程式为8NH3+6NO2$\frac{\underline{\;催化剂\;}}{\;}$7N2+12H2O,
故答案为:8NH3+6NO2$\frac{\underline{\;催化剂\;}}{\;}$7N2+12H2O;
③SO2在O2作用下与NH3、H2O反应形成(NH4)2SO4,此反应中SO2是还原剂,氧气是氧化剂,反应的化学方程式为2SO2+O2+4NH3+2H2O═2(NH4)2SO4,
故答案为:2SO2+O2+4NH3+2H2O═2(NH4)2SO4;
④涉及反应为2NH3+H2SO4=n(NH4)2SO4,2NaOH+H2SO4=Na2SO4+H2O,反应中n(H2SO4)=v1×c1×10-3mol,n(NaOH)=v2×c2×10-3mol,
由方程式可知n(NaOH)+n(NH3)=2n(H2SO4),
则n(NH3)=(2v1×c1×10-3-v2×c2×10-3)mol,
则m(CO(NH2)2)=$\frac{1}{2}$×(2v1×c1×10-3-v2×c2×10-3)mol×60g/mol=(0.06v1c1-0.03v2c2 )g,
尿素溶液中溶质的质量分数是$\frac{0.06{c}_{1}{V}_{1}-0.03{c}_{2}{V}_{2}}{a}×100%$=$\frac{6{c}_{1}{V}_{1}-3{c}_{2}{V}_{2}}{a}%$,
故答案为:$\frac{6{c}_{1}{V}_{1}-3{c}_{2}{V}_{2}}{a}%$;
(2)①由图示可知BaO和NOx反应生成Ba(NO3)2,Ba(NO3)2再还原为N2,则储存NOx的物质为BaO,故答案为:BaO;
②第一步反应中H2被氧化生成水,化合价由0价升高到+1价,Ba(NO3)2的N元素化合价由+5价降低到-3价,生成氨气,则1molBa(NO3)2生成氨气转移16mol电子,参加反应的氢气的物质的量为$\frac{16}{2}$=8mol,则消耗的H2与Ba(NO3)2的物质的量之比是8:1,
故答案为:8:1;
③在有氧条件下15NO与NH3以一定比例反应时,得到的笑气几乎都是15NNO,由N元素守恒可知15NO与NH3应为1:1,可知反应的化学方程式为415NO+4NH3+3O2$\frac{\underline{\;催化剂\;}}{\;}$415NNO+6H2O,
故答案为:415NO+4NH3+3O2;4;6.
点评 本题为2017北京考题,题目以氮氧化物为载体考查元素化合物知识以及化学方程式的相关计算,侧重于学生的分析能力和计算能力的考查,题目难度中等,注意把握题给信息,结合质量守恒计算该题.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | pH=1的溶液:Na+、K+、MnO4-、SO42- | |
| B. | 0.1mol•L-1FeCl3溶液:K+、NH4+、I-、SCN- | |
| C. | 使酚酞变红色的溶液:Na+、Al3+、CO32-、Cl- | |
| D. | 由水电离的c(H+)=1×10-13mol•L-1的溶液:K+、Na+、AlO2-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PM2.5是指粒径不大于2.5μm的可吸入悬浮颗粒物 | |
| B. | 绿色化学要求从源头上消除或减少生产活动对环境的污染 | |
| C. | 燃煤中加入CaO可以减少酸雨的形成及温室气体的排放 | |
| D. | 天然气和液化石油气是我国目前推广使用的清洁燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
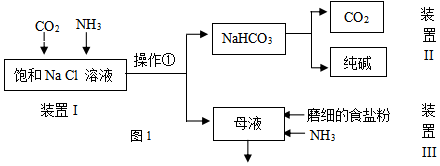
| NaCl | NH4HCO3 | NaHCO3 | NH4Cl | |
| 溶解度(20°C,100gH2O时) | 36.0 | 21.7 | 9.6 | 37.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.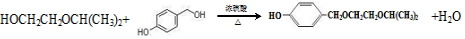 .
.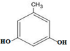 、
、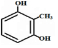 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 夏天设定空调温度尽可能的低 | B. | 推广使用一次性塑料袋和纸巾 | ||
| C. | 少开私家车多乘公共交通工具 | D. | 对商品进行豪华包装促进销售 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
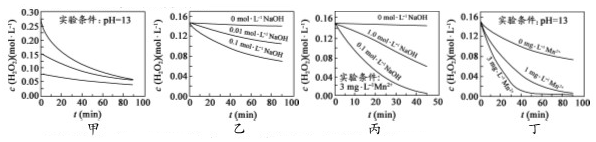
| A. | 图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快 | |
| B. | 图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快 | |
| C. | 图丙表明,少量Mn2+存在时,溶液碱性越强,H2O2分解速率越快 | |
| D. | 图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 装置①可用于实验室制取少量 NH3或 O2 | |
| B. | 可用从 a 处加水的方法检验装置②的气密性 | |
| C. | 实验室可用装置③收集 H2、NH3 | |
| D. | 利用装置④制硫酸和氢氧化钠,其中 b 为阳离子交换膜、c 为阴离子交换膜 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
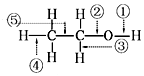
| A. | 当乙醇发生催化氧化时,被破坏的键是②③ | |
| B. | 当乙醇与Na反应时,被破坏的键是① | |
| C. | 当乙醇与乙酸反应时,被破坏的键是② | |
| D. | 当乙醇发生催化氧化时,被破坏的键是①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com