
(12分)通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
|
化学键 |
Si—O |
Si—Cl |
H—H |
H—Cl |
Si—Si |
Si—C |
|
键能/ kJ·mol–1 |
460 |
360 |
436 |
431 |
176 |
347 |
请回答下列问题:
(1)比较下列两组物质的熔点高低(填“>”或“<”)SiC Si;SiCl4 SiO2
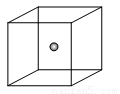
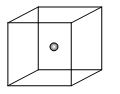
(2)如图立方体中心的“●”表示硅晶体中的一个原子,请在立方体的顶点用“●”表示出与之紧邻的硅原子。
(3)工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g) Si(s)+4HCl(g)
Si(s)+4HCl(g)
该反应的反应热ΔH = kJ·mol–1。
(12分)⑴ >(3分) <(3分)
⑵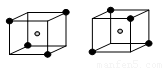 (3分) ⑶ +236 kJ/mol(3分)
(3分) ⑶ +236 kJ/mol(3分)
【解析】(1)SiC和Si形成的晶体都是原子晶体,但由于碳原子半径小于硅原子半径的,所以碳化硅中共价键强于单质硅中的共价键,所以碳化硅的熔点高于硅的熔点;SiCl4形成晶体是分子晶体,而二氧化硅形成的晶体是原子晶体,所以SiCl4的熔点低于二氧化硅的熔点。
(2)晶体硅的结构和金刚石是相似的,即形成的是正四面体形结构,所以结构图可以表示为

(3)反应热就是断键吸收的能量和形成化学键所放出的能量的差值,所以根据方程式可知,该反应的反应热是△H=4×360kJ/mol+2×436kJ/mol-2×176kJ/mol-4×431kJ/mol=+236 kJ/mol。


 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案科目:高中化学 来源:2012-2013年江苏泰州二中高二第一次(10月)限时作业化学试卷(带解析) 题型:填空题
(12分)通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。
| 化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
| 键能/ kJ·mol–1 | 460 | 360 | 436 | 431 | 176 | 347 |
 Si(s)+4HCl(g)
Si(s)+4HCl(g)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com