
【题目】常温下,将NaOH溶液分别滴加到两种一元弱酸HA和HB中,两种混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是

A. Ka(HA)的数量级为10-5
B. 当NaOH溶液与HB混合至中性时:c(B-)<c(HB)
C. 等浓度的NaA、NaB溶液中,水的电离程度:NaA<NaB
D. 等浓度的HB和NaA的混合溶液中:c(Na+)>c(A-)>c(B-)>c(OH-)>c(H+)
【答案】C
【解析】
A. Ka(HA)=![]() ,当c(A-)=c(HA)时,Ka(HA)=c(H+),则Ka(HA)在10-3.0~10-3.5之间,Ka(HA)的数量级为10-4,A错误;
,当c(A-)=c(HA)时,Ka(HA)=c(H+),则Ka(HA)在10-3.0~10-3.5之间,Ka(HA)的数量级为10-4,A错误;
B.根据图知,当溶液中c(B-)=c(HB)时溶液呈酸性,说明HB的电离作用大于B-的水解作用,所以c(B-)>c(HB),B错误;
C.根据图象可知,当溶液中酸分子的浓度等于酸电离产生的离子浓度时,溶液的pH大小关系HA<HB,说明HA电离程度大,即HA的酸性强,根据盐的水解规律可知,等浓度的NaA、NaB溶液中,水的电离程度:NaA<NaB,C正确;
D. NaA是强碱弱酸盐,A-发生水解反应消耗,所以c(Na+)>c(A-),HB是弱酸,存在电离平衡,所以等浓度的盐电离产生的离子浓度大于弱酸电离产生的离子浓度,故c(A-)>c(B-);由于溶液中c(B-)=c(HB)时,溶液呈酸性,又根据选项C分析可知酸性:HA>HB,可见等浓度的HB和NaA的混合溶液显酸性, c(H+)>c(OH-),故该溶液中离子浓度大小关系为:c(Na+)>c(A-)>c(B-)>c(H+)>c(OH-),D错误;
故合理选项是C


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】现有下列反应:
①2H2O+Cl2+SO2=H2SO4+2HCl
②2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
针对上述两个反应回答:
(1)用单线桥标出①中电子转移的方向和数目_____;
(2)写出②的离子化学方程式____;
(3)Cl2、SO2和KMnO4的氧化性由强到弱的顺序为____;
(4)反应②中氯化氢表现出的性质是____。
a.还原性 b.酸性 c.氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.向Ba(OH)2溶液中逐滴加入稀硫酸,请完成下列问题:
(1)写出反应的离子方程式__________。
(2)下列三种情况下,离子方程式与(1)相同的是____(填序号)。
A.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液中显中性
B.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至SO![]() 恰好完全沉淀
恰好完全沉淀
C.向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至过量
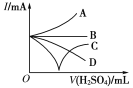
(3)若缓缓加入稀硫酸直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用右图中的___曲线表示(填序号)。
(4)若有一表面光滑的塑料小球悬浮于Ba(OH)2溶液中央,如图所示,向该烧杯里缓缓注入与Ba(OH)2溶液等密度的稀硫酸至恰好完全反应。在此实验过程中,小球将____________。
Ⅱ.某地甲、乙两厂排放污水,污水中含有下列8种离子中的4种:Ag+、Ba2+、Fe3+ 、Na+、Cl-、SO42-、NO3-、OH-(两厂所排污水不含相同离子)。两厂单独排放都会造成严重的水污染(其中甲厂的污水是碱性的),如将两厂的污水按一定比例混合,沉淀后的污水变成无色澄清的几乎只含硝酸钠的溶液而排放,污染程度会大大降低。关于两厂所排污水中所含的4种离子,你认为应该是:甲厂:________;乙厂________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据反应NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl制备碳酸氢钠。下列实验装置能达到实验目的的是

A. 用装置甲制取氨气 B. 用装置乙制取二氧化碳
C. 用装置丙制取碳酸氢钠 D. 用装置丁分离碳酸氢钠与母液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去粗盐中的Ca2+、Mg2+、SO![]() 和泥沙,可将粗盐溶于水,然后进行下列五项操作:
和泥沙,可将粗盐溶于水,然后进行下列五项操作:
①过滤 ②加过量NaOH溶液 ③加适量HCl ④加过量Na2CO3溶液 ⑤加过量BaCl2溶液
通过教材中“粗盐的提纯”及你做过的该实验回答下列问题:
(1)以上五步操作中,最后进行的是________。
(2)实验室进行NaCl溶液的蒸发时,一般有以下操作过程:
①固定铁圈位置 ②放置酒精灯 ③放上蒸发皿(蒸发皿中盛有NaCl溶液) ④加热搅拌 ⑤停止加热
正确的操作顺序为___________________。
(3)在粗盐经过一系列操作后的溶液中滴加过量饱和Na2CO3溶液。请问这步操作的目的是___________________________________________。判断Na2CO3溶液已经过量的方法是_________________________________________________________________。
(4)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的:
溶解时:_________________________________________。
过滤时:_________________________________________。
蒸发时:_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列数量的各物质所含原子数按由大到小的顺序排列的是____。
①0.5 mol氨气 ②标准状况下22.4 L氦气 ③4℃时9 mL水 ④0.2 mol磷酸钠
(2)某双原子分子构成的气体,其摩尔质量为Mg/mol,该气体质量为mg,阿伏加德罗常数为NA,则:
①该气体的物质的量为____mol
②该气体在标准状况下的体积为____L
③该气体在标准状况下的密度为____g/L
④该气体所含原子总数为____个
⑤该气体的一个分子的质量为____g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各选项中,各类物质依次表示为X、Y、Z,其中与图中三个圆所示的从属关系不相符的是:
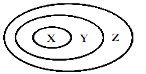
A. 氧化物、化合物、纯净物
B. 碱性氧化物、金属氧化物、氧化物
C. 胶体、分散系、混合物
D. 复分解反应、置换反应、化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组设计利用废旧干电池中的锌皮和未知浓度的稀盐酸制取纯净、干燥的氢气,并验证气体中是否含有杂质。实验装置图如图:
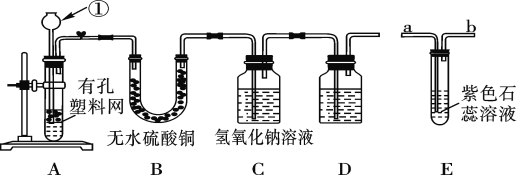
(查阅资料)无水硫酸铜遇水变蓝色。
(1)装置A中仪器①的名称是____;写出发生反应的化学方程式:___。
(2)实验中看到B中无水硫酸铜变蓝色,说明产生的气体中含有杂质水。为了检验气体中还可能存在的杂质,可将E装置连接到上述装置____(填序号)之间,气体从____(填“a”或“b”) 进入装置E。
(3)D装置中的试剂是_____(写出名称)。
(4)下列收集氢气的方法中符合题意的是_____。
A.排水法 B.向下排空气法 C.干瘪的塑料袋 D.塑料瓶
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com