
下列说法正确的是( )
A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH=4
B.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸
C.用0.200 0 mol·L-1 NaOH标准溶液滴定HCl与CH3COOH的混合液(混合液中两种酸的浓度均约为0.1 mol·L-1),至中性时,溶液中的酸未被完全中和
D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1 mol·L-1盐酸、③0.1 mol·L-1氯化镁溶液、④0.1 mol·L-1硝酸银溶液中,Ag+浓度:①>④=②>③
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.高温太阳炉是把热能转变成电能的过程
B.化石燃料燃烧时放出的能量来源于太阳能
C.动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程
D.食用植物体内的淀粉、蛋白质等属直接利用能源
查看答案和解析>>
科目:高中化学 来源: 题型:
从柑橘中可提炼得到结构为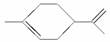 的有机物,下列关于它的说法不正确的是( )
的有机物,下列关于它的说法不正确的是( )
A.分子式为C10H16
B.其一氯代物有8种
C.能与溴水发生加成反应
D.难溶于水,且密度比水大
查看答案和解析>>
科目:高中化学 来源: 题型:
能表明NH3·H2O是弱电解质的叙述是( )
A.NH3·H2O的导电性比NaOH溶液弱得多
B.0.1 mol·L-1NH3·H2O的pH大于7
C.(NH4)2SO4的水溶液,其pH小于7
D.5 mL1 mol·L-1的NH3·H2O跟10 mL0.5 mol·L-1的HCl恰好完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃时,取浓度相同的NaOH和HCl溶液,以32体积比相混合,所得溶液的pH等于12,则原溶液的浓度为( )
A.0.01 mol·L-1 B.0.017 mol·L-1
C.0.05 mol·L-1 D.0.50 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
现有电解质溶液:①Na2CO3 ②NaHCO3 ③NaAlO2 ④CH3COONa ⑤NaOH,且已知:CO2+3H2O+2AlO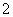 ===2Al(OH)3↓+CO
===2Al(OH)3↓+CO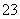 。
。
(1)当五种溶液的pH相同时,其物质的量浓度由大到小的顺序是__________________。
(2)将上述物质的量浓度均为0.1 mol·L-1的五种溶液,稀释相同倍数时,其pH变化最大的是________(填编号)。
(3)在上述五种电解质溶液中,分别加入AlCl3溶液,有气体产生的是________(填编号)。
(4)将上述①②③④四种电解质溶液混合时,发生反应的离子方程式为_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:C(s)+CO2(g)2CO(g) ΔH>0。该反应达到平衡后,下列条件有利于反应向正反应方向进行的是( )
A.升高温度和减小压强
B.降低温度和减小压强
C.降低温度和增大压强
D.升高温度和增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)已知:2NO2(g)N2O4(g) ΔH=-57.20 kJ·mol-1。一定温度下,在密闭容器中反应 2NO2(g)N2O4(g)达到平衡。
其他条件不变时,下列措施能提高NO2的转化率的是________(填字母)。
A.减小NO2的浓度 B.降低温度
C.增加NO2的浓度 D.升高温度
(2)17 ℃、1.01×105Pa,密闭容器中N2O4和NO2的混合气体达到平衡时,c(NO2)=0.030 0 mol·L-1、c(N2O4)=0.012 0 mol·L-1。计算反应2NO2(g)N2O4(g)的平衡常数K。
(3)现用一定量的Cu与足量的浓HNO3反应,制得1.00 L已达到平衡的N2O4和NO2的混合气体(17 ℃、1.01×105Pa),理论上至少需消耗Cu多少克?
查看答案和解析>>
科目:高中化学 来源: 题型:
水热法制备Fe3O4纳米颗粒的反应为3Fe2++2S2O +O2+xOH-===Fe3O4+S4O
+O2+xOH-===Fe3O4+S4O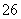 +2H2O,下列说法中错误的是 ( )。
+2H2O,下列说法中错误的是 ( )。
A.每生成1 mol Fe3O4,反应转移的电子总数为4 mol
B.Fe2+和S2O 都是还原剂
都是还原剂
C.1 mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为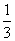 mol
mol
D.x=4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com