
对于反应N2+O2===2NO,在密闭容器中进行,下列条件能加快该反应的速率的是( )
A.增大容器体积
B.体积不变,充入N2使压强增大
C.体积不变,充入He使压强增大
D.压强不变,充入N2使体积增大
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:高中化学 来源: 题型:
已知五种元素的原子序数的大小顺序为C>A>B>D>E;A、C同周期,B、C同主族;A与B形成离子化合物,A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10电子分子。
试回答下列问题:
(1)写出A、B、E元素的名称:A________;B________;E________。
(2)C元素的原子的电子式为________,D元素的原子结构示意图为________,C与E形成的化合物的结构式为________。
(3)写出下列物质的电子式:
A2B2________________;E2B2_______________;
A2C________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某容器中充入H2和N2,在一定条件下合成NH3,下列叙述不正确的是( )
A.开始反应时,正反应的速率最大
B.随着反应的进行,正反应的速率逐渐减小,最终减小为零
C.随着反应的进行,逆反应的速率逐渐增大,后保持不变
D.随着反应的进行,正反应的速率逐渐减小,最终与逆反应的速率相等且保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
将N2、H2的混合气体分别充入甲、乙、丙三个容器后,测得反应速率分别为甲:v(H2)=3 mol/(L·min);乙:v(N2)=2 mol/(L·min);丙:v(NH3)=1 mol/(L·min)。则三个容器中合成氨的速率( )
A.v(甲)>v(乙)>v(丙) B.v(乙)>v(丙)>v(甲)
C.v(丙)>v(甲)>v(乙) D.v(乙)>v(甲)>v(丙)
查看答案和解析>>
科目:高中化学 来源: 题型:
某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mL/L、2.00 mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验HNO3的用量为25.00 mL,大理石用量为10.00 g。
(1)请完成以下实验设计表,并在实验目的一栏中填空:
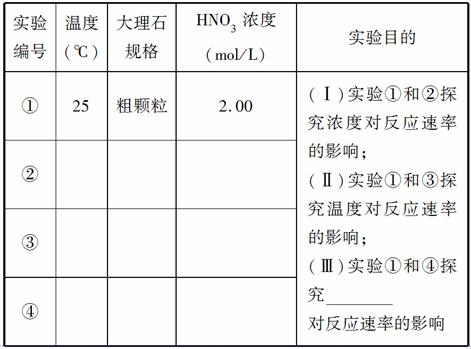
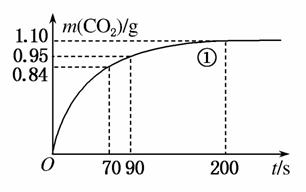
(2)实验①中CO2质量随时间变化的关系见右图。计算实验①中70~90 s范围内用HNO3表示的平均反应速率________(忽略溶液体积变化,不需要写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
分析下面的能量变化示意图,下列热化学方程式正确的是( )
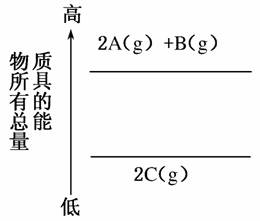
A.2A(g)+B(g)===2C(g) ΔH=a(a>0)
B.2A(g)+B(g)===2C(g) ΔH=a(a<0)
C.2A+B===2C ΔH=a(a<0)
D.2C===2A+B ΔH=a(a>0)
查看答案和解析>>
科目:高中化学 来源: 题型:
所示装置中,观察到电流计指针偏转;M棒变粗;N棒变细。由此判断表中所列M、N、P物质,其中可以成立的是( )
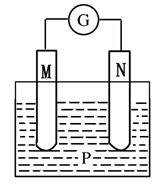
| 选项 | M | N | P |
| A | Zn | Cu | 稀H2SO4溶液 |
| B | Cu | Fe | 稀HCl溶液 |
| C | Ag | Zn | AgNO3溶液 |
| D | Zn | Fe | FeSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:H2(g)+F2(g) === 2HF(g) △H=-270kJ/mol,下列说法正确的是( )
A.1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270kJ
B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于270kJ
C.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量
D.2mol氟化氢气体分解成1mol的氢气和1mol的氟气放出270kJ热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com