
| A. | H2SO4 | B. | KOH | C. | AgNO3 | D. | Na2SO4 |
分析 A、电解硫酸溶液实质是电解水,酸性增强;
B、电解KOH溶液实质是电解水,碱性增强;
C、电解硝酸银产物是硝酸、氧气和银单质;
D、电解硫酸钠溶液实质是电解水,据此回答;
解答 解:A、电解硫酸溶液实质是电解水,酸性增强,电解液的pH减小,故A错误;
B、电解KOH溶液实质是电解水,碱性增强,电解液的pH增大,故B正确;
C、电解硝酸银产物是硝酸、氧气和银单质,溶液从盐溶液成为酸溶液,所以pH减小,故C错误;
D、电解硫酸钠溶液实质是电解水,电解前后溶液的pH几乎不变,故D错误.
故选B.
点评 本题以溶液pH变化为载体考查电解原理,明确发生的反应是解本题关键,易错选项是CD,注意C中虽然没有碱生成,但溶质浓度降低而改变pH,注意D电解后是过饱和溶液而导致pH不变,题目难度中等.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 用30%的H2O2消除面部色斑 | |
| B. | 当不慎在皮肤上沾上少量的浓H2SO4时,应立即用大量水冲洗,并涂上2%的NaHCO3溶液 | |
| C. | 试样$\stackrel{BaCl_{2}}{→}$ 白色沉淀$\stackrel{HCl}{→}$白色沉淀不溶解,则试样中一定有SO42- | |
| D. | 不慎将浓盐酸洒在桌上,应立即用浓NaOH溶液冲洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | MOH和ROH都是强碱 | |
| B. | 稀释前,c(ROH)=10c(MOH) | |
| C. | 在x点,c(M+)=c(R+) | |
| D. | 中和等体积未稀释的MOH和ROH溶液,所需HCl的物质的量:ROH>MOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
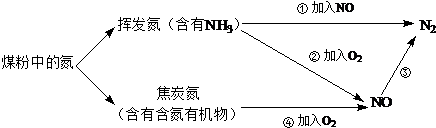
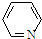 ),其分子中相邻的C和N原子相比,N原子吸引电子能力更强(填“强”或“弱”),从原子结构角度解释原因:C和N在周期表的位置是同一周期从左到右,N 的原子半径更小,原子核对外层电子的吸引力更强.
),其分子中相邻的C和N原子相比,N原子吸引电子能力更强(填“强”或“弱”),从原子结构角度解释原因:C和N在周期表的位置是同一周期从左到右,N 的原子半径更小,原子核对外层电子的吸引力更强.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制备Fe(OH)3胶体后可以用渗析的方法净化 | |
| B. | 利用丁达尔效应可以区分溶液和胶体 | |
| C. | 电泳现象可证明胶体都带电 | |
| D. | 胶体是分散质粒子直径在1~100nm之间的分散系 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 血红素中含有C、H、O、N、Fe五种元素.回答下列问题:
血红素中含有C、H、O、N、Fe五种元素.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.
到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com