
小资料:1775年法国化学家拉瓦锡在定量研究空气组成时,发现从空气中分离得到N2的密度与分离含氮物质得到N2的密度之间总有一个微小的差异,但这并没引起他的注意.一百多年后,英国科学家雷利对这0.0064 g·cm-3的差异进行了分析,几经努力,他终于发现在空气中还存在着一种懒惰的气体——氩气,从而发现了惰性气体家族.
(1)阅读资料,你有哪些感受?
(2)下面是科学家雷利在实验探究中的几个重要步骤,请补充完整:
问题与猜想→( )![]() 分析与结论
分析与结论![]() ( )
( )
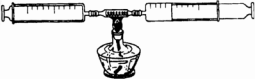
(3)某同学在探究空气成分中氧气的含量时,模拟了科学家的探究过程.他设计了如下实验:在由两个注射器组成的密闭容器内留有25 mL空气,给装有细铜丝的玻璃管加热(如图).请你与之合作,继续完成该实验的探究.
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案科目:高中化学 来源: 题型:




查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
 以色列化学家丹尼尔?谢赫经因为发现准晶体而获得2011年诺贝尔化孚奖.准晶体原子里排列有序,但不具备普通晶体的长程平移对称性,而且原子位置之间有间隙(如图).下列说法不正确的是( )
以色列化学家丹尼尔?谢赫经因为发现准晶体而获得2011年诺贝尔化孚奖.准晶体原子里排列有序,但不具备普通晶体的长程平移对称性,而且原子位置之间有间隙(如图).下列说法不正确的是( )| A、石墨是原子晶体,0.12g石墨中约含6.02×1021个碳原子 | B、与类似普通晶体比较,准晶体延展性较低 | C、与类似将通晶体比较,准晶体密度较小 | D、普通玻璃属于非晶体,其成份中存在共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分) 铬是1979年法国化学家沃克兰在分析铬铅矿时首先发现的,位于周期表中第四周期ⅥB族,其主要化合价为+6、+3、+2,其中其中+3较为稳定。我校化学兴趣小组对铬的化合物进行探究性研究。
Ⅰ、查阅资料
(1)Cr2O3微溶于水,与Al2O3类似,是两性氧化物;Cr(OH)3和Al(OH)3类似,也是两性氢氧化物。
(2)工业上和实验室中常见的铬(+6价)化合物是其含氧酸盐,如铬酸盐和重铬酸盐,以K2Cr2O7和Na2Cr2O7最为重要。工业废水中含有Cr3+,可以通过加入石灰,降低溶液的酸度,当PH为8~9时,Cr3+能形成沉淀而分离。
Ⅱ、工业上为了处理含有Cr2O72-的酸性工业废水,采用下面的处理方法:往工业废水中加入适量的NaCl,以Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)3沉淀生成,使废水中的铬含量达排放标准。
①在装置中应该用 (填材料名称)做电解池的阳极。能否用石墨做电极,说明原因______________________________________________________________,
阴极上电极反应方程式是 。
②Cr2O72- 在酸性条件下有强氧化性,试写出Cr2O72-转变成Cr3+的离子方程式。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com