
【题目】下列指定微粒的数目相等的是
A.等物质的量的12CO2与14CO2含有的中子数
B.同温、同压、同体积的CO2和N2O含有的质子数
C.等质量的己烷和丁烷中含有的共用电子对数
D.等物质的量的钠和铁分别与足量氯气完全反应时转移的电子数
【答案】B
【解析】
A.一个12CO2分子中含中子为6+8×2=22,一个14CO2分子中含中子为8+8×2=24,则物质的量相等的12CO2与14CO2含有的中子数比值为22:24,中子数不同,故A错误;
B.同温同压下,其体积之比=物质的量之比=分子个数之比,一个CO2分子含有的质子数为6+8×2=22,一个N2O分子含有的质子数为7×2+8=22,所以二者的质子数相等,故B正确;
C.1个己烷中共用电子对数为19,1个丁烷中共用电子对数为13,等质量的己烷和丁烷共用电子对数比为:![]() ×19:
×19:![]() ×13=1102:1118,等质量的己烷和丁烷中含有共用电子对数不相同,故C错误;
×13=1102:1118,等质量的己烷和丁烷中含有共用电子对数不相同,故C错误;
D.等物质的量的钠和铁分别与足量氯气完全反应生成等物质的量的氯化钠、氯化铁,产物中钠离子是+1价,铁离子是+3价。则转移的电子数不相等,故D错误;
答案为B。


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
【题目】某工厂对制革工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+):
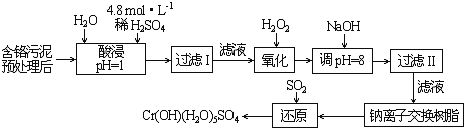
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.0 | -- | -- | 4.7 | -- |
沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9(>9溶解 |
(1)实验室用18.4molL-1的浓硫酸配制250mL4.8molL-1的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和移液管(一种能精确量取一定体积液体的仪器)外,还需___。
(2)酸浸时,为了提高浸取率可采取的措施是___(至少两条)。
(3)加入H2O2的作用是___。
(4)钠离子交换树脂的原理为:Mn++nNaR→MRn+nNa+,被交换的杂质离子是___。
(5)还原过程发生以下反应(请配平):__Na2Cr2O7+__SO2+__=__Cr(OH)(H2O)5SO4+__Na2SO4;
(6)从流程的滤液中可回收的主要物质是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机化合物的用途及性质的说法正确的是
A.乙烯使酸性KMnO4溶液或溴的CCl4溶液褪色的原理相同
B.苯与液溴在催化剂作用下生成溴苯发生了加成反应
C.淀粉、蛋白质等营养物质在人体内水解生成水和CO2等
D.用K2Cr2O7检验司机是否酒驾利用了乙醇的挥发性和还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下进行反应:COCl2(g)![]() Cl2 (g)+CO(g)。向2.0 L恒容密闭容器中充入1.0 mol COCl2 (g),经过一段时间后达到平衡。反应过程中测得的有关数据见下表:
Cl2 (g)+CO(g)。向2.0 L恒容密闭容器中充入1.0 mol COCl2 (g),经过一段时间后达到平衡。反应过程中测得的有关数据见下表:
t/s | 0 | 2 | 4 | 6 | 8 |
n(Cl2) /mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
下列说法正确的是 ( )
A.保持其他条件不变,升高温度,平衡时c(Cl2) = 0.22 mol·L-1,则反应的 △H < 0
B.若在2 L恒容绝热(与外界没有热量变换)密闭容器进行该反应,化学平衡常数不变
C.保持其他条件不变,起始向容器中充入1.2 mol COCl2、0.60 mol Cl2和0.6 mol CO,反应达到平衡前的速率:v (正) > v (逆)
D.保持其他条件不变,起始向容器中充入1.0 mol Cl2和0.8 mol CO,达到平衡时,Cl2的转化率小于60%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)只用水就能鉴别的一组物质是______
a.苯、乙酸、四氯化碳 b.乙醇、乙醛、乙酸
c.乙醛、乙二醇、硝基苯 d.苯酚、乙醇、甘油
(2)现有化合物:甲: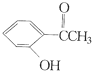 乙:
乙: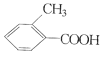 丙:
丙: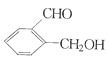
①请写出丙中含氧官能团的名称:____。
②请判别上述哪些化合物互为同分异构体:____(填代号)。
(3)A和B两种物质的分子式都是C7H8O芳香族化合物,它们都能跟金属Na反应放出H2;A不溶于NaOH溶液而B能溶于NaOH溶液,B能使FeCl3溶液显紫色,A不能;B苯环上的一溴代物有两种结构。则A和B的名称及结构简式为:A_____,B_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸松油酯是松油醇的酯化产物,具有甜香气味,广泛应用于日用和食用香精中。乙酸松油酯的结构简式如图甲所示,下列说法正确的是
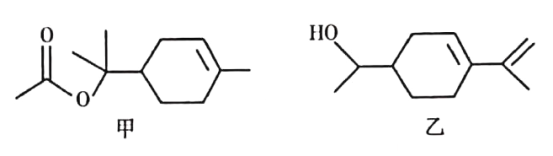
A. 乙酸松油酯的分子式为C12H22O2
B. 乙酸松油酯的水解产物松油醇与图乙所示物质互为同分异构体
C. 乙酸松油酯既易溶于水、也易溶于乙醇或油脂
D. 乙酸松油酯能使Br2的CCl4溶液或酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米级Fe3O4呈黑色,因其有磁性且粒度小而在磁记录材料、生物功能材料等诸多领域有重要应用,探究其制备和用途意义重大。
(1)还原-沉淀法:①用还原剂Na2SO3将一定量Fe3+可溶盐溶液中的![]() Fe3+还原,使Fe2+和Fe3+的物质的量比为1 : 2。②然后在①所得体系中加入氨水,铁元素完全沉淀形成纳米Fe3O4。写出②过程的离子方程式:__________。
Fe3+还原,使Fe2+和Fe3+的物质的量比为1 : 2。②然后在①所得体系中加入氨水,铁元素完全沉淀形成纳米Fe3O4。写出②过程的离子方程式:__________。
(2)电化学法也可制备纳米级Fe3O4,用面积为4 cm2的不锈钢小球(不含镍、铬)为工作电极,铂丝作阴极,用Na2SO4溶液作为电解液,电解液的pH维持在10左右,电流50 mA。生成Fe3O4的电极反应为______。
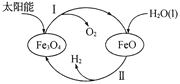
(3)已知:H2O(1) === H2(g)+![]() O2(g) △H =+285.5 kJ·mol-l,以太阳能为热源分解Fe3O4,经由热化学铁氧化合物循环分解水制H2的过程如下,完善以下过程I的热化学方程式。过程I:__________。过程Ⅱ:3FeO(s)+H2O(l) === H2(g)+Fe3O4(s) △H =+128.9 kJ·mol-1
O2(g) △H =+285.5 kJ·mol-l,以太阳能为热源分解Fe3O4,经由热化学铁氧化合物循环分解水制H2的过程如下,完善以下过程I的热化学方程式。过程I:__________。过程Ⅱ:3FeO(s)+H2O(l) === H2(g)+Fe3O4(s) △H =+128.9 kJ·mol-1
(4)磁铁矿(Fe3O4)常作冶铁的原料,主要反应为Fe3O4(s)+4CO(g)![]() 3Fe(s)+4CO2 (g),该反应的△H < 0,T℃时,在1 L恒容密闭容器中,加入Fe3O4、CO各0.5 mol,10 min后反应达到平衡时,容器中CO2的浓度是0.4 mol·L-1。
3Fe(s)+4CO2 (g),该反应的△H < 0,T℃时,在1 L恒容密闭容器中,加入Fe3O4、CO各0.5 mol,10 min后反应达到平衡时,容器中CO2的浓度是0.4 mol·L-1。
①T℃时,10 min内用Fe3O4表示的平均反应速率为___g·min-1。
②T℃时,该反应的平衡常数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.既有单质参加又有单质生成的反应一定是氧化还原反应
B.发生了颜色变化的一定是化学变化
C.用鸡蛋壳膜和蒸馏水除去淀粉胶体中的食盐不涉及化学变化
D.根据丁达尔现象可以将分散系分为溶液、胶体和浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于离子共存或离子反应的说法正确的是( )
A.某无色溶液中可能大量存在H+、Cl-、MnO4-
B.pH=2的溶液中可能大量存在Na+、NH4+、SiO32-
C.Fe2+与H2O2在酸性溶液中的反应:2Fe2++H2O2+2H+=2Fe3++2H2O
D.稀硫酸与Ba(OH)2溶液的反应:H++SO42-+Ba2++OH-=BaSO4↓+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com